题目内容
9.微观粒子看不见、摸不着,科学家通过模型来说明他们心目中粒子的“模样”,揭示物质的微观结构特点,解释微观结构与宏观现象之间的因果关系.模型化的方法是化学科学重要的思想工具,试回答下列问题:(1)原子的结构
一百多年来,化学有借助构建原子结构模型,逐渐揭开了原子构成的神秘面纱,并通过不断提出新的原子结构模型,逐步形成了今天的原子结构理论.
①如图1两种模型是汤姆生和卢瑟福分别于1897年和1911年提出的,其中A(填代号,下同)是由汤姆生提出的.
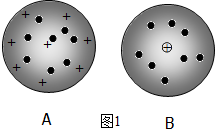
②下列关于原子结构理论的学说中,汤姆生的观点是BCDG(填代号,下同),卢瑟福的观点是BCEFGH.
A、原子是不可分的
B、原子是可分的
C、原子呈球形
D、在球体内充斥着正电荷,电子镶嵌其中
E、带正电荷的原子核居于原子的中心
F、带正电荷的原子核很小,但集中了原子的大部分质量
G、电子带负电
H、电子在原子核外很大的空间内高速运动
(2)离子的结构
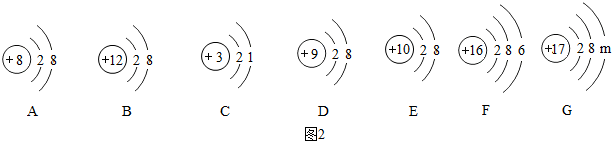
在初中化学中,离子的结构可以用离子结构示意图来表示,在图中:
①A、B、D中属于阳离子的是B(填代号,下同),属于阴离子的是AD;
②C、F形成的化合物中,它们的化合价分别应该是+1、-2.
③若G表示某元素原子,则m=7,该元素的原子在化学反应中容易得到(选填“得到”或“失去”)电子.
(3)分子的结构(如图3小圆球分别表示碳原子、氢原子、氧原子)
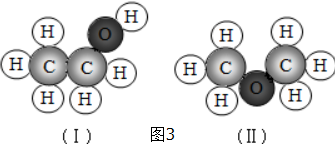
图中(Ⅰ)和(Ⅱ)分别是两个分子的微观结构模型,你认为它们所代表的物质的化学式是否相同?相同.
分析 (1)道尔顿认为原子是坚实的、不可再分的实心球,后来汤姆森通过实验发现了电子,他认为原子中存在更小的微粒,原子是可分的,并提出类似“西瓜”的原子模型,认为电子就像“西瓜子”一样镶嵌在带正电荷的“西瓜瓤”中;卢瑟福的原子核式结构模型:在原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间里绕着核旋转;
(2)阳离子的核内质子数小于核外电子数;阴离子的核内质子数大于核外电子数;从原子结构示意图进行分析;
(3)比例模型可以直观地表示分子的形状,其碳原子的成键情况是确定分子结构的关键,碳原子的成键情况主要根据与碳原子形成共价键的原子的数目确定,原子半径的关系为C>O>H
解答 解:(1)①道尔顿认为原子是坚实的、不可再分的实心球,后来汤姆森通过实验发现了电子,他认为原子中存在更小的微粒,原子是可分的,并提出类似“西瓜”的原子模型,认为电子就像“西瓜子”一样镶嵌在带正电荷的“西瓜瓤”中;卢瑟福的原子核式结构模型:原子是一个空心的球,在原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间里绕着核旋转.故答案为:A;
②根据汤姆森和卢瑟福理论分析可知,BCDG代表汤姆森的观点;BCEFGH代表卢瑟福的观点,故答案为:BCDG;BCEFGH;
(2)①阳离子的核内质子数小于核外电子数;阴离子的核内质子数大于核外电子数;②从C和F的原子结构看,C易失去一个电子,F易得到两个电子,故它们的化合价分别应该是+1价和-2价;③根据原子结构的表示方法,G的质子数为17,则其有三个电子层,由里向外每层的电子数为2,8,7,故m=7,最外层电子数大于4,易得电子;故答案为:①B;AD;②+1;-2;③7;得到;
(3)CH3-CH2-OH和CH3-O-CH3的化学式相同,但结构不同,不是同种物质;故答案为:相同.
故答案为:(1)①A;②BCDG;BCEFGH;(2)①B;AD;②+1;-2;③7;得到;(3)相同.
点评 本题考查原子、离子、分子的结构知识,基础性强.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | O2 | B. | CO2 | C. | 水蒸气 | D. | N2 |
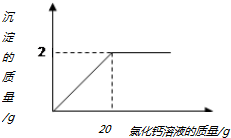 小林在做实验时发现,实验室的纯碱样品中混入了少量的食盐,为测定该纯碱样品中碳酸钠的含量,小明称取该纯碱样品2.5g,再滴加氯化钙溶液至不再产生沉淀,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示
小林在做实验时发现,实验室的纯碱样品中混入了少量的食盐,为测定该纯碱样品中碳酸钠的含量,小明称取该纯碱样品2.5g,再滴加氯化钙溶液至不再产生沉淀,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示