题目内容
13.某黑色固体粉末可能是Fe、FeO、CuO、C中一种或几种.为了探究其成分,小明同学按照如图所示流程进行了实验.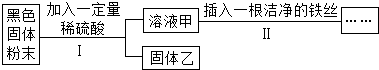
关于该实验有以下说法正确的是( )
| A. | 若溶液甲呈浅绿色,则原黑色固体粉末中一定含有Fe | |
| B. | 若步骤Ⅱ中无明显现象,则固体乙中最多有五种物质 | |
| C. | 若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO | |
| D. | 若固体乙呈红色,则原固体中一定含有Fe和CuO |
分析 根据C不与稀硫酸反应;氧化铜可以与稀硫酸反应,生成的Cu2+在水溶液中显蓝色;Fe可以与稀硫酸反应生成气体;Fe、FeO与硫酸反应生成的Fe2+在水溶液中显浅绿色;铁的活动性大于铜,能将铜从其盐溶液中置换出来,据此分析判断有关的说法.
解答 解:由于C不与稀硫酸反应;氧化铜可以与稀硫酸反应,生成的Cu2+在水溶液中显蓝色;Fe可以与稀硫酸反应生成气体;Fe、FeO与硫酸反应生成的Fe2+在水溶液中显浅绿色;铁的活动性大于铜,能将铜从其盐溶液中置换出来.
A、若溶液甲呈浅绿色,则原黑色固体粉末中不一定含有Fe,FeO也可以与稀硫酸反应生成的Fe2+在水溶液中显浅绿色;故A错误;
B、若步骤Ⅱ中无明显现象,说明了溶液中无硫酸铜,没有剩余的硫酸,如果硫酸的量不足,则固体乙中最多可以有Fe、FeO、CuO、C、Cu五种物质,故B正确;
C、若步骤Ⅱ中有红色固体析出,说明了溶液中含有硫酸铜,能判断黑色粉末中含有CuO,不能判断固体乙中是否有CuO,故C错误;
D、固体乙呈红色,说明有铁置换出的铜,则原固体中一定含有Fe和CuO.故D正确.
故选BD.
点评 同学们需要掌握常见离子、物质的颜色,如:Cu2+显蓝色,Fe2+显绿色,Fe3+显黄色,Cu显红色等.

练习册系列答案
相关题目
3.学习化学我们要经常做实验,错误操作会给我们带来危险和误差,你认为下列实验操作正确的是 ( )
| A. | 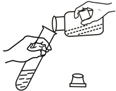 倾倒试剂 | B. |  滴加试剂 | C. | 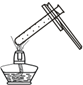 液体加热 | D. | 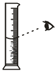 量筒读数 |
1.我国第四套人民币硬币中使用到镍(Ni)、铜、铁等金属.某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序.
(1)【查阅资料】镍能与稀硫酸反应,生成可溶于水的NiSO4,并放出氢气.
①写出镍与稀硫酸反应的化学方程式Ni+H2SO4=NiSO4+H2↑.
②结合所学知识,不能(填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
(2)【探究实验】(所用金属片均已用砂纸打磨.)
(3)【实验反思】用镍片、硫酸亚铁溶液和CuSO4(填化学式)溶液通过实验也能判断Fe、Ni、Cu的金属活动性顺序.
(4)【迁移应用】某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,此外还有一些不溶性杂质.若废液直接排放到下水道不仅造成重金属污染,而且造成浪费,该校化学兴趣小组同学设计了如图废液处理方案,请回答有关问题:

①废液在加入金属X前需进行过滤,过滤时需要将圆形滤纸折叠处理.如图示中不该出现的情况是C.

②加入过量金属X发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu,溶液Y是稀硫酸.
(1)【查阅资料】镍能与稀硫酸反应,生成可溶于水的NiSO4,并放出氢气.
①写出镍与稀硫酸反应的化学方程式Ni+H2SO4=NiSO4+H2↑.
②结合所学知识,不能(填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
(2)【探究实验】(所用金属片均已用砂纸打磨.)
| 实验步骤 | 实验现象 | 结 论 |
 | 铁片表面有固体析出, 铜片表面无明显现象 | 三种金属活动性由强到弱的顺序为Fe>Ni>Cu |
(4)【迁移应用】某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,此外还有一些不溶性杂质.若废液直接排放到下水道不仅造成重金属污染,而且造成浪费,该校化学兴趣小组同学设计了如图废液处理方案,请回答有关问题:

①废液在加入金属X前需进行过滤,过滤时需要将圆形滤纸折叠处理.如图示中不该出现的情况是C.

②加入过量金属X发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu,溶液Y是稀硫酸.
 分析图中NaCl、KNO3的溶解度曲线,回答问题
分析图中NaCl、KNO3的溶解度曲线,回答问题