题目内容
18.实验室有一瓶含有硫酸的废液,老师请小红同学设计方案测定该废液中硫酸的溶质质量分数.小红同学先取一洁净小烧杯,称其质量为16.2g,然后往其中倒入少量硫酸废液后称量,总质量为56.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去掉铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为66.8g.请回答下列问题:
(1)写出上述反应的化学方程式:Fe+H2SO4=FeSO4+H2↑.
(2)反应中产生的气体的质量是0.2 g.
(3)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数).
(4)如果铁钉的铁锈未除净,对计算结果的影响是偏小 (选填“偏大”、“偏小”、“无影响”),原因是硫酸与铁锈反应.
分析 (1)根据铁和稀硫酸反应生成硫酸亚铁和氢气,写出反应的化学方程式;
(2)利用质量差可以求生成氢气的质量;
(3)根据氢气的质量求出硫酸中溶质的质量,从而求出废液中硫酸的质量分数即可.
(4)根据硫酸与铁锈的反应分析对计算结果的影响.
解答 解:(1)铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑;
(2)完全反应后,容器中的物质的质量差,就是生成氢气的质量,氢气的质量为:56.2g+10.8g-66.8g=0.2g;
(3)设与铁反应的硫酸的质量为x,
烧杯中稀硫酸废液的质量为:56.2g-16.2g=40g
Fe+H2SO4═FeSO4+H2↑
98 2
x 0.2g
$\frac{98}{x}=\frac{2}{0.2g}$
x=9.8g
该废液中硫酸的质量分数=$\frac{9.8g}{40g}×$100%=24.5%
(4)由于硫酸与铁锈的反应,如果铁钉的铁锈未除净,对计算结果的影响是偏小.
故答为:(1)Fe+H2SO4=FeSO4+H2↑;(2)0.2; (3)该废液中硫酸的质量分数是24.5%;(4)偏小,硫酸与铁锈反应.
点评 本题主要考查有关化学方程式的计算,难度较小.根据质量的变化求出生成氢气的质量是进行有关计算的基础.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
8. 测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.
测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.
(1)根据下表提供的实验数据,计算出该实验测得的氧气在空气中体积分数?
小明:这道题很简单不就是用15mL减去7mL属于消耗的氧气的体积,再用氧气的体积除以注射器内反应前总气体的体积吗.
小亮:你说的不对,应该是用消耗的氧气的体积除以硬质玻璃管中空气的体积.
…
你的意见是:反应前注射器中空气体积不能忽略.
实验反思:
(2)气球在导管的最右侧比较合理,理由是缓冲,防止试管内气体温度升高,气压增大,冲开橡皮塞.
 测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.
测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.(1)根据下表提供的实验数据,计算出该实验测得的氧气在空气中体积分数?
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 7mL | 20% |
小亮:你说的不对,应该是用消耗的氧气的体积除以硬质玻璃管中空气的体积.
…
你的意见是:反应前注射器中空气体积不能忽略.
实验反思:
(2)气球在导管的最右侧比较合理,理由是缓冲,防止试管内气体温度升高,气压增大,冲开橡皮塞.
9.金属Ni、Mn分别放入其他三种金属X、Y、Z的盐溶液中,反应的结果和有无金属析出的情况如下表所示.
它们的金属活动性由强到弱的顺序为( )
| X盐溶液 | Y盐溶液 | Z盐溶液 | |
| Ni | 无 | 无 | 有 |
| Mn | 无 | 有 | 有 |
| A. | X Mn Y Ni Z | B. | Z Ni Y Mn X | ||
| C. | Z Mn Y Ni X | D. | X Mn Ni Y Z |
13.某黑色固体粉末可能是Fe、FeO、CuO、C中一种或几种.为了探究其成分,小明同学按照如图所示流程进行了实验.
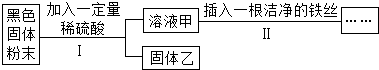
关于该实验有以下说法正确的是( )

关于该实验有以下说法正确的是( )
| A. | 若溶液甲呈浅绿色,则原黑色固体粉末中一定含有Fe | |
| B. | 若步骤Ⅱ中无明显现象,则固体乙中最多有五种物质 | |
| C. | 若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO | |
| D. | 若固体乙呈红色,则原固体中一定含有Fe和CuO |
7.很多商场、健身俱乐部等公众场合,明文规定“不得在室内吸烟”.有人在室内吸烟,不吸烟的人也能闻到烟味的原因是( )
| A. | 分子很小 | B. | 分子之间有间隙 | C. | 分子在不断运动 | D. | 分子由原子构成 |
8.“食品安全”大于天,下列有关做法中,正确的是( )
| A. | 用化工染色剂制作“彩色馒头” | B. | 用甲醛浸泡白菜根部防腐烂 | ||
| C. | 用回收的食用油重复炸制食品 | D. | 适量的小苏打用于制作面包 |
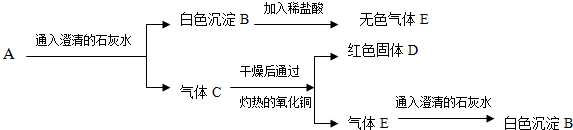
 已知A、B、C、D、E是初中化学中常见的五种物质,均含有同一种元素.其中A、E为固体物质,B和C含有的元素完全相同,D是一种酸,E是一种重要建筑材料的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答:
已知A、B、C、D、E是初中化学中常见的五种物质,均含有同一种元素.其中A、E为固体物质,B和C含有的元素完全相同,D是一种酸,E是一种重要建筑材料的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答: