题目内容
11.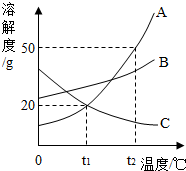 如图为A、B、C三种固体物质的溶解度曲线,请回答
如图为A、B、C三种固体物质的溶解度曲线,请回答(1)溶解度变化受温度影响最大的物质是A.
(2)t2℃时,溶解度最小的物质是C.
(3)把接近饱和的B溶液转化为饱和溶液,可采用的方法降低温度(写1种).
(4)t1℃时,将50gA物质加入100g水中,充分搅拌后形成的溶液属于饱和(填“饱和”或“不饱和”)溶液;若要使该溶液中溶质的质量分数增大,你采用的可行方法是升高温度.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,溶解度变化受温度影响最大的物质是A;
(2)t2℃时,溶解度最小的物质是C;
(3)B物质的溶解度随温度的降低而减小,所以把接近饱和的B溶液转化为饱和溶液,可采用的方法降低温度;
(4)t1℃时,A物质的溶解度是20g,所以将50gA物质加入100g水中,充分搅拌后形成的溶液属于饱和溶液;若要使该溶液中溶质的质量分数增大,你采用的可行方法是升高温度.
故答案为:(1)A;
(2)C;
(3)降低温度;
(4)饱和,升高温度.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列有关海水综合利用的说法正确的是( )
| A. | 电解氯化镁溶液可得到金属镁 | |
| B. | 海水晒盐得到食盐后的母液可用于提取多种化工原料 | |
| C. | 海水中含有碘元素,只需将海水中的碘升华就可以得到碘单质 | |
| D. | 利用潮汐发电是将化学能转化为电能 |
2.有关水的认识正确的是( )
| A. | 电解水得到H2和O2,可知水是由氢原子和氧原子组成的 | |
| B. | 生活中用过滤的方法可以降低水的硬度 | |
| C. | 净水的方法有沉淀、过滤、吸附、蒸馏 | |
| D. | 经过自来水厂处理的水是纯水 |
6.下列四种生活现象中,与其他三种有本质区别的是( )
| A. |  玻璃碎了 | B. |  划火柴 | ||
| C. |  蜡烛熔化 | D. |  |
16.甲同学在做铁与流速溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了如下探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
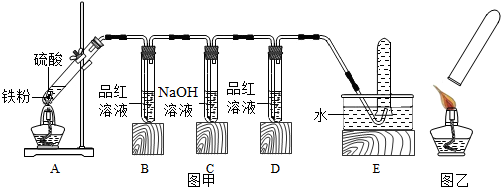
请帮助小明填写如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫.
【反思】
(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;.
(2)实验一中C装置的作用是吸收二氧化硫.发生的反应的化学方程式:SO2+2NaOH═Na2SO3+H2O.
【拓展延伸】
(3)实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助小明填写如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | SO2、H2都有 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【反思】
(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;.
(2)实验一中C装置的作用是吸收二氧化硫.发生的反应的化学方程式:SO2+2NaOH═Na2SO3+H2O.
【拓展延伸】
(3)实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
20.生产、生活离不开化学知识.下列做法或行为中,正确的是( )
| A. | 用粮食酿造的米醋作调味剂 | |
| B. | 杜绝吃含有化学物质的食品 | |
| C. | 随意进入废弃的矿洞内游玩 | |
| D. | 在不通风的澡室里用燃气热水器洗澡 |
1.化学是一门以实验为基础的科学,借助科学的实验方法,我们可以从不同角度正确地认识物质.
(1)探究微粒的性质:如图1所示,烧杯B中的现象是由无色液体变红色;,产生这一现象体现了分子的性质为分子不断地运动;
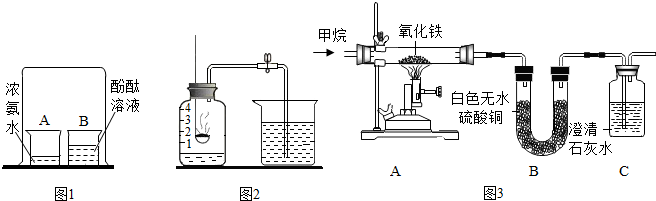
(2)探究物质的组成:图2所示实验可用于测定空气的组成.实验中能说明空气中氧气含量为五分之一的现象为:红磷燃烧结束后,冷却到室温,打开止水夹,烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)探究物质的性质:小军按图3探究甲烷的性质,他查阅资料获知白色无水硫酸铜遇水会变蓝,请完成下面的实验报告:
(1)探究微粒的性质:如图1所示,烧杯B中的现象是由无色液体变红色;,产生这一现象体现了分子的性质为分子不断地运动;

(2)探究物质的组成:图2所示实验可用于测定空气的组成.实验中能说明空气中氧气含量为五分之一的现象为:红磷燃烧结束后,冷却到室温,打开止水夹,烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)探究物质的性质:小军按图3探究甲烷的性质,他查阅资料获知白色无水硫酸铜遇水会变蓝,请完成下面的实验报告:
| 实 验 现 象 | 实 验 结 论 |
| A中红色粉末变为黑色; B中白色无水硫酸铜变蓝色; C中澄清石灰水变浑浊. | 反应的产物为二氧化碳、水, 甲烷具有还原性,A中反应的化学方程式为 3CH4+4Fe2O3$\frac{\underline{\;高温\;}}{\;}$8Fe+6H2O+3CO2 |
 A~F均为初中化学常见的物质,已知:A、C是组成元素完全相同的化合物,C通常为液体,D为无色气体,F是白色难溶固体,其中金属元素的质量分数为40%.它们之间有如图所示的转化关系(部分物质和反应条件已略去).
A~F均为初中化学常见的物质,已知:A、C是组成元素完全相同的化合物,C通常为液体,D为无色气体,F是白色难溶固体,其中金属元素的质量分数为40%.它们之间有如图所示的转化关系(部分物质和反应条件已略去).