题目内容
13.为检验一无色溶液,进行如下实验:滴入紫色石蕊试液会变红色,加入铁片会产生能燃烧的气体;再往原溶液中加入少量的氯化钡溶液产生不溶于稀硝酸的白色沉淀.(1)这一无色溶液是硫酸;
(2)有关反应的化学方程式是:①Fe+H2SO4=FeSO4+H2↑;②H2SO4+BaCl2=BaSO4↓+2HCl.
分析 根据无色溶液中滴入紫色石蕊试液会变红色,所以该溶液显酸性,加入铁片会产生能燃烧的气体,所以该溶液中含有氢离子,再往原溶液中加入少量的氯化钡溶液产生不溶于稀硝酸的白色沉淀,所以该溶液中含有银离子和硫酸根离子,所以该无色溶液是硫酸,然后进行验证即可.
解答 解:(1)无色溶液中滴入紫色石蕊试液会变红色,所以该溶液显酸性,加入铁片会产生能燃烧的气体,所以该溶液中含有氢离子,再往原溶液中加入少量的氯化钡溶液产生不溶于稀硝酸的白色沉淀,所以该溶液中含有银离子和硫酸根离子,所以该无色溶液是硫酸,经过验证,推导正确,所以这一无色溶液是硫酸;
(2)硫酸和铁反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,化学方程式为:H2SO4+BaCl2=BaSO4↓+2HCl.
故答案为:(1)硫酸;
(2)Fe+H2SO4=FeSO4+H2↑;
H2SO4+BaCl2=BaSO4↓+2HCl.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.如表除杂质的方法错误的是( )
| 物质(括号内为杂质) | 除杂方法 | |
| A | NaCl(泥沙) | 溶解、过滤、蒸发 |
| B | FeCl2(CuCl2) | 加入适量铁粉 |
| C | CaCl2溶液(盐酸) | 加入过量CaCO3 |
| D | CO2(CO) | 通入澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
18. 实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
(l)根据步骤①现象,小明得出了该试剂可能为氯化钠溶液或硫酸钠溶液.小明作出该判断的依据是步骤①的实验现象是“无色酚酞试液不变色”.
(2)由步骤②可确定该试剂为硫酸钠溶液.
 实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:| 步骤 | 实验操作 | 实验现象 |
| ① | 取5毫升试剂于A试管中,滴入几滴无色酚酞试液 | 无色酚酞试液… |
| ② | 另取5 毫升试剂于B 试管中,滴入几滴氯化钡溶液 | 溶液中出现白色沉淀 |
(2)由步骤②可确定该试剂为硫酸钠溶液.
5.已知氯化银(白色)、碳酸银(白色)、碳酸钙(白色)、氢氧化铜(蓝色)都难溶于水.下列溶液分别跟氯化铜溶液、稀盐酸、碳酸钠溶液反应,并产生不同现象的是( )
| A. | NaOH | B. | H2SO4 | C. | AgNO3 | D. | Ca(OH)2 |
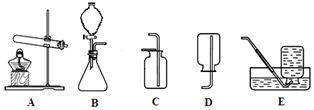
 人类的生活离不开金属,用我们学到的化学知识和方法能分析和解释许多现象.
人类的生活离不开金属,用我们学到的化学知识和方法能分析和解释许多现象. 利用如图实验装置,某同学做了如下两个探究实验:
利用如图实验装置,某同学做了如下两个探究实验: