题目内容
3.NO是工业制硝酸的中间产物,生成NO的化学方程式为4X+5O2 $\frac{\underline{MnO_2}}{△}$4NO+6H2O,据此可以推断出X的化学式为NH3.分析 根据化学变化前后原子的种类、个数不变,由反应的化学方程式4x+5O2$\frac{\underline{MnO_2}}{△}$4NO+6H2O,可推断反应物X的分子构成,确定反应物X的化学式
解答 解:由反应的化学方程式4x+5O2$\frac{\underline{MnO_2}}{△}$4NO+6H2O,根据化学变化前后原子的种类、个数不变,可判断物质x的4个分子中含有4个氮原子、12个氢原子,则物质x的分子由1个氮原子、3个氢原子所构成,因此物质x的化学式为NH3;
故填:NH3.
点评 通过书写化学方程式及利用化学方程式推断物质的化学式,本题对化学方程式的书写及意义进行基础考查.

练习册系列答案
相关题目
13.推理时学习化学的常见方法,以下推理合理的是( )
| A. | 二氧化锰是氯酸钾分解反应的催化剂,任何分解反应都可用二氧化锰做催化剂 | |
| B. | 金刚石和石墨都是碳的单质,金刚石很硬,故石墨也很硬 | |
| C. | 高锰酸钾受热分解可以产生氧气,所以能分解产生氧气的物质一定含有氧元素 | |
| D. | 氧化物中一定含有氧元素,含有氧元素的物质一定是氧化物 |
14.下面和空气混合后不可能发生爆炸的是( )
| A. | 面粉 | B. | 天然气 | C. | 氮气 | D. | 汽油 |
11.鉴别CO和H2的最好方法是( )
| A. | 闻气体的气味 | B. | 点燃观察火焰的颜色 | ||
| C. | 点燃后检验其生成物 | D. | 溶解于水 |
18.下列说法正确的是( )
| A. | “绿色食品”都是绿色的植物 | |
| B. | 植物的光合作用有益于生态平衡 | |
| C. | 吸烟会危害人体健康,但不会污染环境 | |
| D. | 发电厂热水直接排入江河,有利于鱼类生存 |
15.如表是某城市某日空气质量报告:
某研究性学习小组对表中首要污染物S02:导致酸雨的成因进行探究.
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.
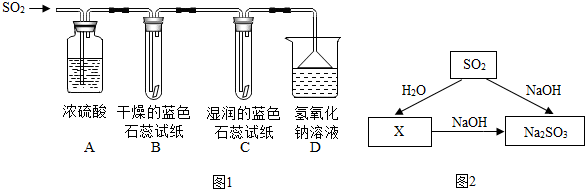
(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | S02 | Ⅱ | 良 |
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.

(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
12.下列叙述中正确的是( )
| A. | 二氧化碳分子是由一个碳原子和一个氧分子构成的 | |
| B. | 分子一定比原子大 | |
| C. | 不同元素的原子的核电荷数一定不同 | |
| D. | 核外电子排布相同的粒子一定属于同一种元素 |
13.自来水是我国目前主要的生活饮用水,下表是我国颁布的生活饮用水水质标准的部分内容:
(1)感官指标表现的是自来水的物理(填“物理”或“化学”)性质.
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH 6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1, 氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.