题目内容
13.推理时学习化学的常见方法,以下推理合理的是( )| A. | 二氧化锰是氯酸钾分解反应的催化剂,任何分解反应都可用二氧化锰做催化剂 | |
| B. | 金刚石和石墨都是碳的单质,金刚石很硬,故石墨也很硬 | |
| C. | 高锰酸钾受热分解可以产生氧气,所以能分解产生氧气的物质一定含有氧元素 | |
| D. | 氧化物中一定含有氧元素,含有氧元素的物质一定是氧化物 |
分析 A.根据催化剂的定义及二氧化锰的性质来完成解答;
B.石墨和金刚石组成元素相同,金刚石和石墨的原子排列方式不同,所以两者的物理性质不相同;
C.根据质量守恒定律解答;
D.氧化物是指由两种元素组成且其中一种是氧元素的化合物.
解答 解:A.二氧化锰在过氧化氢分解的反应中是催化剂,但是在其它的反应中不一定是催化剂,故错误;
B.石墨和金刚石组成元素相同,金刚石和石墨的原子排列方式不同,所以两者的物理性质不相同,故错误;
C.根据质量守恒定律,化学反应前后元素的种类不变,高锰酸钾受热分解可以产生氧气,所以能分解产生氧气的物质一定含有氧元素,故正确;
D.氧化物中一定含有氧元素,但是含氧元素的化合物不一定属于氧化物,如氢氧化钠含氧元素,但却是由Na、O、H三种元素组成的化合物不属于氧化物,故错误.
故选C.
点评 本题考查的是对常见的概念的推理,完成此题,可以依据已有的概念进行.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
3.下列物质中,随着温度的升高,在水中的溶解度减小的是( )
| A. | 熟石灰 | B. | 食盐 | C. | 硝酸钾 | D. | 氢氧化钠 |
4. 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.
(1)硫酸是化学实验中常备的试剂,从化工商店买回来的一般是浓硫酸,某浓硫酸标签上的部分内容如图所示.如果要配制1kg10%的稀硫酸,需要这种浓硫酸的体积约为54.3mL(结果精确到0.1mL).配制稀硫酸时,正确的操作是先将量取的900mL水倒入烧杯中,然后将量取的54.3mL浓硫酸沿着烧杯壁慢慢注入水中,并不断的用玻璃棒进行搅拌.(2)氢氧化钠是一种常见的碱,俗名苛性钠、火碱或烧碱.请写出一条氢氧化钠在工业上的用途造纸、纺织、制肥皂等.
(3)为探究“酸碱中和反应”,某班同学进行了如下实验,将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【提出问题】实验中无明显现象反应后溶液中的溶质是什么?
【做出猜想】①只有Na2SO4;②Na2SO4和H2SO4;③Na2SO4和NaOH;④Na2SO4、H2SO4和NaOH
不合理的猜想是④.
【实验探究】取烧杯中的溶液于试管中,滴加CuSO4溶液后无明显变化,则溶液中一定没有NaOH,为了验证其余猜想,同学们进行了如下三个实验方案的探究:
【结论与反思】通过探究,可确定猜想②是正确的,请指出以上实验探究中存在的两处错误pH试纸浸入溶液中,BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
(4)完全中和溶质质量分数为5%的氢氧化钠溶液16g,需溶质质量分数为4.9%的稀硫酸多少克?
 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.(1)硫酸是化学实验中常备的试剂,从化工商店买回来的一般是浓硫酸,某浓硫酸标签上的部分内容如图所示.如果要配制1kg10%的稀硫酸,需要这种浓硫酸的体积约为54.3mL(结果精确到0.1mL).配制稀硫酸时,正确的操作是先将量取的900mL水倒入烧杯中,然后将量取的54.3mL浓硫酸沿着烧杯壁慢慢注入水中,并不断的用玻璃棒进行搅拌.(2)氢氧化钠是一种常见的碱,俗名苛性钠、火碱或烧碱.请写出一条氢氧化钠在工业上的用途造纸、纺织、制肥皂等.
(3)为探究“酸碱中和反应”,某班同学进行了如下实验,将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【提出问题】实验中无明显现象反应后溶液中的溶质是什么?
【做出猜想】①只有Na2SO4;②Na2SO4和H2SO4;③Na2SO4和NaOH;④Na2SO4、H2SO4和NaOH
不合理的猜想是④.
【实验探究】取烧杯中的溶液于试管中,滴加CuSO4溶液后无明显变化,则溶液中一定没有NaOH,为了验证其余猜想,同学们进行了如下三个实验方案的探究:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 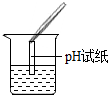 | 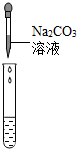 | 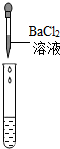 |
| 实验现象 | 试纸变色,对比标准比色卡:pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(4)完全中和溶质质量分数为5%的氢氧化钠溶液16g,需溶质质量分数为4.9%的稀硫酸多少克?
8.“地球是我家,环境保护靠大家!”下列标志,与保护环境无关的是( )
| A. |  禁止燃放鞭炮 | B. |  | C. |  | D. |  |