题目内容
2.碳捕捉与碳封存技术可以抽离出大气中的CO2,用于储存和生产有用的产品,从而减少碳排放,某化学课题小组,用NaOH溶液“捕捉”CO2模拟处理废气.若废气中CO2的质量分数为88%,其余为水蒸气,当废气通过NaOH溶液时CO2被完全“捕捉”,并恰好消耗20%的氢氧化钠溶液80g(假定废气完全进入溶液),计算:(1)“捕捉”的CO2的质量;
(2)最后溶液中Na2CO3的质量分数.
分析 二氧化碳和氢氧化钠反应生成碳酸钠和水,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)设“捕捉”的CO2的质量为x,生成碳酸钠质量为y,
2NaOH+CO2═Na2CO3+H2O,
80 44 106
80g×20% x y
$\frac{80}{80g×20%}$=$\frac{44}{x}$=$\frac{106}{y}$,
x=8.8g,y=21.2g,
答:“捕捉”的CO2的质量为8.8g.
(2)设废气中水的质量为z,
根据题意有:(8.8g+z)×88%=8.8g,
z=1.2g,
最后溶液中Na2CO3的质量分数为:$\frac{21.2g}{80g+10g}$×100%=23.6%,
答:最后溶液中Na2CO3的质量分数为23.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
13.下列化学方程式的书写正确的是( )
| A. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | Cu+AgNO3=Cu( NO3 )2+Ag | ||
| C. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | D. | 2Fe+6HCl=2FeC13+3H2↑ |
10.为了安全,下列说法或做法正确的是( )
| A. | 家用天然气若泄露,不能立即点火或打开电源开关 | |
| B. | 稀释浓硫酸时,将水沿器壁缓缓注入浓硫酸中,并不断搅拌 | |
| C. | 若氢氧化钠溶液沾在皮肤上,应立即涂上稀盐酸 | |
| D. | 冬天室内用煤火取暖,在炉上放一壶水能防止煤气中毒 |
7.下列说法中,你认为正确的是( )
| A. | 催化剂能改变化学反应的速率,对生成物的质量没有影响 | |
| B. | 施用化肥可使农作物增加产量,不会造成环境污染 | |
| C. | 正常人呼吸的氧气越多、越纯,身体就越健康 | |
| D. | 由于矿物燃料的燃烧,二氧化碳在大气中的含量在不断增加 |
2.日常生活中,燃烧现象屡见不鲜.小华设计了如下实验方案来探究燃烧的条件:
(1)用镊子分别夹取一根小木条和一块小石子,在酒精灯上点燃.
(2)用镊子分别夹取一个蘸有水、一个没蘸水的小棉花团,放到酒精灯火焰上片刻.
(3)分别点燃两枝小蜡烛,将其中一枝蜡烛用玻璃杯罩住.
分析实验:请帮助小华将未完成的实验报告填写完整:
得出结论:
燃烧需要三个条件:可燃物;温度要达到着火点;与氧气接触.
(1)用镊子分别夹取一根小木条和一块小石子,在酒精灯上点燃.
(2)用镊子分别夹取一个蘸有水、一个没蘸水的小棉花团,放到酒精灯火焰上片刻.
(3)分别点燃两枝小蜡烛,将其中一枝蜡烛用玻璃杯罩住.
分析实验:请帮助小华将未完成的实验报告填写完整:
| 实验步骤 | 设计意图 | 实验现象 | 实验结论 |
| (1) | 燃烧与物质的关系 | 可燃物才能燃烧 | |
| (2) | 燃烧与温度的关系 | 没蘸水的小棉花团燃烧,蘸水的小棉花团没燃烧 | |
| (3) | 玻璃杯内蜡烛熄灭了,玻璃杯外蜡烛仍燃烧 |
燃烧需要三个条件:可燃物;温度要达到着火点;与氧气接触.
3.根据要求回答有关问题:
(1)从上表Ⅰ组的备选答案中,写出跟“二氧化硫、五氧化二磷、二氧化碳”属于同一类物质的化学式H2O;
(2)小明认为Ⅱ组中的Si与其他三种不属于同类物质,你认为其理由是硅属于非金属单质,其他三种物质属于金属单质.
| 组别 | A | B | C | D |
| Ⅰ组 | 水 | 氧气 | 硫酸铜 | 氯化钾 |
| Ⅱ组 | Fe | Na | Al | Si |
(2)小明认为Ⅱ组中的Si与其他三种不属于同类物质,你认为其理由是硅属于非金属单质,其他三种物质属于金属单质.

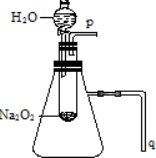 用脱脂棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱酯棉上滴水.可观察到脱脂棉剧烈燃烧起来
用脱脂棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱酯棉上滴水.可观察到脱脂棉剧烈燃烧起来