题目内容
20.下列实验方案中,不能证明NaOH溶液与稀盐酸发生了反应的是( )| A. | 向一定量的NaOH溶液中通入CO2后再滴加稀盐酸,有气体生成 | |
| B. | 向装有一定量NaOH溶液的烧杯中滴几滴酚酞溶液,再逐滴加入稀盐酸 | |
| C. | 先测定NaOH溶液的pH,再逐滴加入稀盐酸,溶液的pH数值逐渐降低 | |
| D. | 向装有少量稀盐酸的试管中滴加足量NaOH溶液,再向其中滴加Na2CO3溶液 |
分析 根据证明NaOH溶液与稀盐酸发生了反应,可通过证明溶液的酸碱性发生了改变,结合酸与碱的化学性质,进行分析判断.
解答 解:A、向一定量的NaOH溶液中通入CO2后,二氧化碳与氢氧化钠反应生成碳酸钠和水,有气体生成,是因为碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,不能证明NaOH溶液与稀盐酸发生了反应,故选项正确.
B、向装有一定量NaOH溶液的烧杯中滴几滴酚酞溶液,逐滴加入稀盐酸,至溶液由红色变为无色,证明NaOH溶液与稀盐酸发生了反应,故选项错误.
C、先测定NaOH溶液的pH,pH大于7,再逐滴加入稀盐酸,溶液的pH数值逐渐降低,证明NaOH溶液与稀盐酸发生了反应,故选项错误.
D、向装有少量稀盐酸的试管中滴加足量NaOH溶液,再向其中滴加Na2CO3溶液,没有气泡产生,证明NaOH溶液与稀盐酸发生了反应,故选项错误.
故选:A.
点评 本题难度不大,明确可通过溶液的酸碱性发生了改变证明发生了中和反应是正确解答本题的关键.

练习册系列答案
相关题目
4.下列物质与对应的标志不相符的是( )
| A. |  白磷 | B. |  酒精 | C. |  浓硫酸 | D. |  碳酸钠 |
15.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如下图所示:
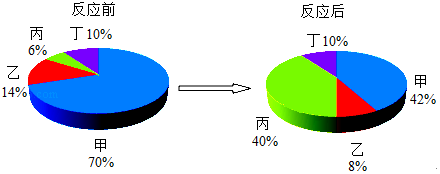
下列说法正确的是( )

下列说法正确的是( )
| A. | 乙可能是单质 | |
| B. | 在该反应中丁一定没有参加化学反应 | |
| C. | 该反应可能是置换反应 | |
| D. | 甲和乙的质量之和一定等于生成丙的质量 |
5.已知金属X与CuSO4反应的化学方程式为2X+CuSO4═X2SO4+Cu,下列说法中不正确的是( )
| A. | 该反应为置换反应 | |
| B. | 金属X在金属活动性顺序表里一定在Cu前面 | |
| C. | 金属X可能是Fe | |
| D. | 反应前后,硫元素的化合价没有发生改变 |
12.晓铭在实验室中发现了一瓶碳酸钠和氯化钠的混合液.他想测定该混合液中碳酸钠和氯化钠的质量分数,并为此设计了如下实验:取该混合液50g,向其中逐滴加入稀盐酸.当加入的稀盐酸的质量为20g、40g、60g 时,生成气体的质量如下表所示.(气体的溶解度忽略不计)求:
(1)当混合液中的碳酸钠完全反应时,生成气体的质量为4.4g.
(2)该混合液中碳酸钠的质量分数.
| 加入的稀盐酸(g) | 20 | 40 | 60 |
| 生成气体的质量(g) | 2.2 | 4.4 | 4.4 |
(2)该混合液中碳酸钠的质量分数.
9.将一定质量的镁、锌混合物粉末放入到一定质量的硫酸铜溶液中,待反应停止后,过滤得滤渣和滤液,再向滤渣中加入足量的稀盐酸,滤渣部分溶解且有气体生成,则下列说法正确的是( )
| A. | 滤渣中一定有镁、铜 | |
| B. | 滤渣中一定有镁、锌、铜 | |
| C. | 滤液中一定有硫酸铜和硫酸锌 | |
| D. | 滤液中一定有硫酸镁,一定没有硫酸铜 |
 (1)葡萄糖酸钙相对分子质量为430;
(1)葡萄糖酸钙相对分子质量为430;