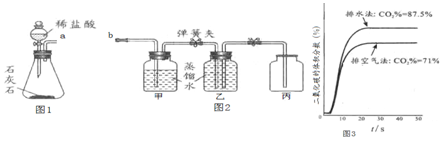
题目内容
5.已知金属X与CuSO4反应的化学方程式为2X+CuSO4═X2SO4+Cu,下列说法中不正确的是( )| A. | 该反应为置换反应 | |
| B. | 金属X在金属活动性顺序表里一定在Cu前面 | |
| C. | 金属X可能是Fe | |
| D. | 反应前后,硫元素的化合价没有发生改变 |
分析 A、一种单质和一种化合物反应生成另外一种单质和另外一种化合物,这种反应属于置换反应;
B、金属活动性顺序表中,排在前面的金属,能够把排在它后面的金属从它的盐溶液中置换出来;
C、铁能和硫酸铜反应生成硫酸亚铁和铜;
D、化合物中元素化合价代数和为零.
解答 解:A、反应物和生成物都是一种单质和一种化合物,属于置换反应,该选项说法正确;
B、X能够把铜从它的盐溶液中置换出来,说明X比铜活泼,该选项说法正确;
C、铁和硫酸铜反应的化学方程式为:Fe+CuSO4═FeSO4+Cu,因此X不能是铁,该选项说法不正确;
D、反应前后,硫元素的化合价没有发生改变,都是+6,该选项说法正确.
故选:C.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
16.用饱和食盐水和碳酸氢铵反应可以获得碳酸氢钠:NH4HCO3+NaCl═NaHCO3↓+NH4Cl(20℃时,NH4HCO3溶解度为21g,NaCl溶解度为36g,NaHCO3溶解度为9.6g).下列关于该反应的叙述正确的是( )
| A. | NaHCO3是碱 | |
| B. | 该反应中四种物质都是盐 | |
| C. | 该反应不符合复分解反应发生的条件 | |
| D. | 析出晶体后剩余溶液中的溶质只有NH4Cl一种 |
13.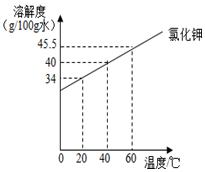 根据下表实验,回答相关问题
根据下表实验,回答相关问题
①实验步骤Ⅱ中加入Xg氯化钾,X=9g.
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
 根据下表实验,回答相关问题
根据下表实验,回答相关问题| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃. | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和. | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热 | 全部溶解 |
| Ⅴ | 冷却至20℃ | 有固体析出 |
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
20.下列实验方案中,不能证明NaOH溶液与稀盐酸发生了反应的是( )
| A. | 向一定量的NaOH溶液中通入CO2后再滴加稀盐酸,有气体生成 | |
| B. | 向装有一定量NaOH溶液的烧杯中滴几滴酚酞溶液,再逐滴加入稀盐酸 | |
| C. | 先测定NaOH溶液的pH,再逐滴加入稀盐酸,溶液的pH数值逐渐降低 | |
| D. | 向装有少量稀盐酸的试管中滴加足量NaOH溶液,再向其中滴加Na2CO3溶液 |
 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题. “孔明灯”又叫天灯(如图所示).一般的孔明灯是用竹片架成圆桶形,外面以薄纸密密包围且开口朝下.欲点灯升空时,在底部的支架中间绑上一块沾有煤油或酒精的粗布,放飞前将粗布点燃,感觉到孔明灯的薄纸膨胀变轻后便放手,随后整个灯就会冉冉升空.若某孔明灯选用的燃料为酒精(C2H5OH),请写出酒精完全燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
“孔明灯”又叫天灯(如图所示).一般的孔明灯是用竹片架成圆桶形,外面以薄纸密密包围且开口朝下.欲点灯升空时,在底部的支架中间绑上一块沾有煤油或酒精的粗布,放飞前将粗布点燃,感觉到孔明灯的薄纸膨胀变轻后便放手,随后整个灯就会冉冉升空.若某孔明灯选用的燃料为酒精(C2H5OH),请写出酒精完全燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.