题目内容
2.地球上的金属资源大多以化合物的形式存在,还原法是冶炼金属的常用方法.请写出用一氧化碳从赤铁矿(主要成分为氧化铁)中冶炼铁的化学方程式Fe2O3+3CO$\frac{\underline{\;点燃\;}}{\;}$2Fe+3CO2.铁在自然环境中很容易生锈,请写出一种防止钢铁制品锈蚀的方法涂油、电镀、刷漆等.分析 根据炼铁的原理和书写化学方程式的步骤完成;在钢铁表面涂油、刷漆等,是利用了隔绝空气和防水的原理,都能防治钢铁生锈.
解答 解:一氧化碳和赤铁矿(主要成分是氧化铁)反应后生成铁和二氧化碳,条件是高温,故反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;点燃\;}}{\;}$2Fe+3CO2;
在钢铁表面喷漆、涂刷矿物油或镀上其他金属等覆盖保护膜的方法防止生锈.故答案为:Fe2O3+3CO$\frac{\underline{\;点燃\;}}{\;}$2Fe+3CO2;涂油、电镀、刷漆等.
点评 本题考查了炼铁的原理,锈蚀条件及其防护,属于结合课本知识的信息.要知道金属锈蚀的条件和防止金属制品生锈的措施,并结合生活实际.

练习册系列答案
相关题目
12.治疗手足口病的常用药物阿昔洛韦化学式为C8H11N5O3.下列有关阿昔洛韦的说法正确的是( )
| A. | 该物质不属于有机化合物 | |
| B. | 阿昔洛韦中碳元素的质量分数为$\frac{12×8}{12×8+11×1+14×5+16×3}$×100% | |
| C. | 阿昔洛韦中 C、H、N、O 三种元素的质量比为8:11:5:3 | |
| D. | 阿昔洛韦是由8个碳原子,11个氢原子,5个氮原子,3个氧原子构成的 |
13.下列化学符号所表示的意义错误的是( )
| A. | H2:可以表示一个氢气分子 | B. | Cu2+:可以表示铜单质 | ||
| C. | S:可以表示一个硫原子 | D. | H2O:可以表示水这种物质 |
10.下列物质的化学式书写不正确的是( )
| A. | 三氧化硫 SO3 | B. | 氯化铁 FeCl3 | C. | 硫酸钠 Na2SO4 | D. | 氧化铝 AlO2 |
7.按要求填写下表.
| 物质名称 | 硫 | 氦气 | 氧化亚铁 | 硫酸 | 氢氧化钾 |
| 化学式 | S | He | FeO | H2SO4 | KOH |
14.下列与化学有关的知识内容正确的是( )
| A. | H2、CH4都是可燃气体--点燃前须检验纯度 | |
| B. | 水污染--对人类没有影响 | |
| C. | 油锅着火时用水浇灭 | |
| D. | 鉴别硝酸铵和硫酸铵--加熟石灰研磨,闻气味 |
11.根据如表回答相关问题.
①表中两种物质的溶解度相等的温度范围是在20~40℃.
②20℃时,硝酸钾的溶解度是31.6g/100g水,其含义是20℃时100g水中溶解31.6g硝酸钾达到饱和.该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是65.8g.要进一步提高该溶液的溶质质量分数,可进行的操作是加热.
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是冷却热饱和溶液.
④60℃时,对100g硝酸钾饱和溶液(如A烧杯)进行如下操作,请回答相关问题:

上述溶液中所含溶质的质量D=E(填“>”或“<”或“=”,下同),溶液不饱和的是 C(用A、B、C、D、E填空),溶液B、C、E中溶质质量分数的大小关系是B=E>C.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
②20℃时,硝酸钾的溶解度是31.6g/100g水,其含义是20℃时100g水中溶解31.6g硝酸钾达到饱和.该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是65.8g.要进一步提高该溶液的溶质质量分数,可进行的操作是加热.
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是冷却热饱和溶液.
④60℃时,对100g硝酸钾饱和溶液(如A烧杯)进行如下操作,请回答相关问题:

上述溶液中所含溶质的质量D=E(填“>”或“<”或“=”,下同),溶液不饱和的是 C(用A、B、C、D、E填空),溶液B、C、E中溶质质量分数的大小关系是B=E>C.
12.下列实验操作中,能达到实验目的是( )
| A. |  干燥氨气 | B. | 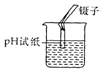 测定某溶液的pH | ||
| C. | 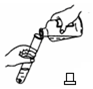 向试管中倾倒液体 | D. | 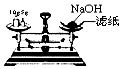 称取氢氧化钠固体 |