题目内容
4. 人类的日常生活和工农业生产离不开水,请回答:
人类的日常生活和工农业生产离不开水,请回答:Ⅰ.用如图所示的净水器处理浑浊的河水,(净水器中有石英砂、活性炭、纱布等)
,下列分析正确的是AD.
A、净化后的河水属于混合物
B、该净水器能将硬水变为软水
C、该净水器能杀菌消毒
D、用活性炭可以除去水中的色素和异味.
Ⅱ.海水占了全球水资源的97%,海水资源的开发和利用具有非常广阔的前景,海水中含有大量的NaCl,可用于制备 实验,其流程如图:

(1)用提纯得到的“精盐”配制100g7.5%的氧化钠溶液,经检测,溶质质量分数偏小,其原因可能有①②(填序号)
①氯化钠固体不纯②称量时精盐与砝码放反了③量取水时俯视读数④装瓶时,有少量溶液洒出
(2)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:

①过滤后得到的白色沉淀的化学式是Mg(OH)2.
②若实验过程中不考虑损耗,最终到的NaCl固体的质量将大于(填“大于”、“小于”或“等于”)原精盐中NaCl的质量.
分析 Ⅰ.分析简易净水器中各层物质的作用可知:小卵石可过滤河水中较大的不溶性固体颗粒,石英沙可除去较小的不溶性固体颗粒,活性炭主要吸附杂质、色素等杂质,蓬松棉用于防止过滤层随水漏下;经过此装置只能除去水中的不溶性固体杂质和异味,不能除去其中的细菌、微生物、钙镁化合物等,得不到纯净的水;Ⅱ.(1)据此结合题意进行分根据氯化钠溶液的质量分数偏小,可能是氯化钠质量少了,也可能是水的质量多了进行分析;
(2)①根据氢氧化钠和氯化镁会生成氢氧化镁沉淀进行分析;
②根据氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠进行分析判断.
解答 解:Ⅰ.A、要达到净化后的水属于纯净物的效果,应进行蒸馏操作,该装置净化后得到的水中含有可溶性的钙镁化合物等,属于混合物,不是蒸馏水,故选项说法错误.
B、要达到将硬水变为软水的效果,需要降低水中钙、镁离子含量,通过煮沸或蒸馏,而该装置不能除去水中的可溶性钙镁化合物,不能降低水的硬度,故选项说法错误.
C、要达到杀菌消毒的效果,需要加入消毒剂,而图示净水器中不含有消毒剂,则该净水器不能起到杀菌消毒的效果,故选项说法错误.
D、活性炭具有吸附作用,可以除去水中的色素和异味,故选项说法正确;
Ⅱ.(1)氯化钠溶液的质量分数偏小,可能是氯化钠质量少了,也可能是水的质量多了;
①氯化钠固体不纯,会导致氯化钠质量偏小,溶质质量分数偏小,故①正确;
②称量时精盐与砝码放反了,氯化钠质量等于砝码质量-游码质量,会导致氯化钠质量偏小,溶质质量分数偏小,故②正确;
③量取水时俯视读数,导致水的质量偏小,溶质质量分数偏大,故③错误;
④装瓶时,有少量溶液洒出,溶质质量分数不变,故④错误.
故选:①②;
(2)①氢氧化钠和氯化镁会生成氢氧化镁沉淀,所以白色沉淀的化学式为Mg(OH)2;
②氢氧化钠和氯化镁会生成氯化钠,盐酸和氢氧化钠也会生成氯化钠,所以实验过程中不考虑损耗,最终到的NaCl固体的质量将大于原精盐中NaCl的质量;
故答案为:Ⅰ.AD;
Ⅱ.(1)①②;
(2)①Mg(OH)2;②大于.
点评 本题难度不大,考查了简易净水器和粗盐提纯、溶液配制的相关知识,掌握净化水的原理、明确提纯每一步的反应原理是正确解答本题的关键,能较好考查学生分析、解决问题的能力.

| A. | 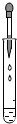 滴加液体 | B. | 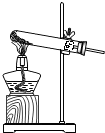 加热液体 | ||
| C. | 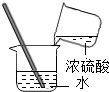 稀释浓硫酸 | D. | 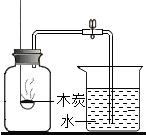 测定空气中氧气的含量 |

| A. | 该反应属于复分解反应 | |
| B. | 四种物质中只有一种是氧化物 | |
| C. | 参加反应的甲、乙分子数之比为1:1 | |
| D. | 反应前后元素的化合价都发生了改变 |
| A. | 钙是人体必需的元素,要注意合理摄入,摄入不足或过量均不利于人体健康 | |
| B. | 从海水中获得物质都需经过化学变化 | |
| C. | 将化学能转化为电能,比转化为内能更有效洁净环保 | |
| D. | 维生素在人体内可以起到调节新陈代谢、预防疾病和维持身体健康的重要作用 |
| A. |  柠檬pH=1.5 | B. |  苹果pH=4.1 | C. |  菠萝pH=5.1 | D. |  柿子pH=8.5 |
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉,并过滤 |
| ③ | H2 | CO2 | 通过盛有NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| ④ | NaCl | CaCO3 | 溶解、过滤、蒸发 |
| A. | ①②③④ | B. | ③④ | C. | ②③④ | D. | ①②③ |
 如图所示.将蜡烛与绿色植物一起放在黑暗密闭的玻璃罩内,一个月后观察到的现象是( )
如图所示.将蜡烛与绿色植物一起放在黑暗密闭的玻璃罩内,一个月后观察到的现象是( )| A. | 植物活着、蜡烛熄灭 | B. | 植物死亡、蜡烛燃尽 | ||
| C. | 植物活着、蜡烛燃尽 | D. | 植物死亡、蜡烛熄灭 |

