题目内容
14.今年我市的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题.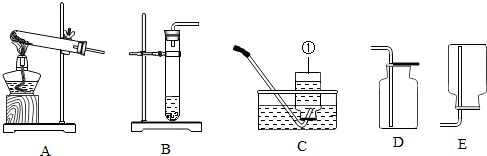
(1)指出标号①的仪器名称集气瓶;
(2)实验室制取二氧化碳选用的发生装置和收集装置依次为B、D(填序号),反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 (1)根据常见的化学仪器的名称进行分析解答.
(2)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置.
解答 解:(1)标号①的仪器名称是集气瓶.
(2)在实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,所以应该选择D装置来收集二氧化碳.
实验室常用大理石或石灰石和与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:(1)集气瓶;(2)B、D;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.

练习册系列答案
相关题目
4.下列有关物质的检验方法与结论都合理的是( )
| A. | 加入稀盐酸,有无色气体产生的物质中一定有碳酸盐 | |
| B. | 经点燃,产生蓝色火焰的气体不一定是一氧化碳 | |
| C. | 能使紫色石蕊试液变红的一定是酸 | |
| D. | 用燃着的木条深入某气体中,火焰熄灭,则该气体一定是二氧化碳 |
5.下列物质露置于空气中,一段时间后,质量增加的是( )
| A. | 浓硫酸 | B. | 双氧水 | C. | 浓盐酸 | D. | 烧碱 |
2.环潭中心学校九(8)的章强同学用氢氧化钙和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究.请你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙.
猜想二:溶质中有CaCl2和Ca(OH)2.
猜想三:溶液中有氯化钙和氯化氢.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
【方案反思】方案一不能证明猜想一正确的理由是酚酞试液在中性溶液和酸性溶液中都不变色(或盐酸和氯化钙的混合溶液也不能使酚酞变色).
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向烧杯中的溶液中加入碳酸钙,直到不再溶解,过滤得氯化钙溶液.
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑可能过量的反应物.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙.
猜想二:溶质中有CaCl2和Ca(OH)2.
猜想三:溶液中有氯化钙和氯化氢.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入碳酸钠(或碳酸钾)溶液至过量 | 开始有气泡产生,后来有白色沉淀生成 | 猜想三正确 |
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向烧杯中的溶液中加入碳酸钙,直到不再溶解,过滤得氯化钙溶液.
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑可能过量的反应物.
9.HNO3中氮元素的化合价为( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
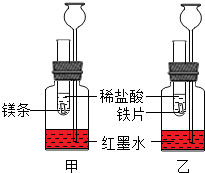 在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.