题目内容
3.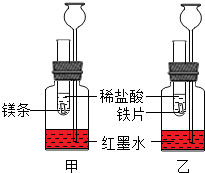 在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.(1)该实验的目的之一是比较镁、铁与稀盐酸反应的剧烈程度.两支长颈漏斗中产生的现象不同之处是甲装置长颈漏斗中的液面比乙装置中的高.
(2)反应结束后,若甲、乙装置中产生的H2质量相等,一定没有剩余的物质是盐酸.
分析 从提供的药品和装置的特点来分析实验目的.活动性强的金属与酸反应剧烈,单位时间内放出的热量多,由此可推知反应现象;根据“若甲、乙装置中产生的H2质量相等”、“稀盐酸的质量和质量分数均相等”,推测剩余的物质.
解答 解:(1)所给的金属在外形上相同,酸的质量分数相同,因此是比较镁、铁与稀盐酸反应的剧烈程度的;从装置图看出,都是密闭的系统,为了观察水被压入漏斗中的量,因此是比较相同时间内镁、铁与稀盐酸反应放出热量的多少的;因为镁和酸反应快,放出的热量多,所以甲装置长颈漏斗中的液面比乙装置中的高;
(2)反应结束后,若甲、乙装置中产生的H2质量相等,又因为“稀盐酸的质量和质量分数均相等”,故一定没有剩余的物质是盐酸.
故答案为:
(1)目的:比较镁、铁与稀盐酸反应的剧烈程度或比较相同时间内镁、铁与稀盐酸反应放出热量的多少; 不同之处:甲装置长颈漏斗中的液面比乙装置中的高
(2)盐酸
点评 本题从不同角度分析实验过程中的各个环节,从实验目的到实验现象,到实验结果,很有深度;
根据金属的活动性顺序判断,过滤用到的仪器和实验数据的处理进行分析.

练习册系列答案
相关题目
13.化学用语是学习化学的工具,下列化学符号中的数字表示的意义不正确的( )
| A. | SO2:“2”表示一个二氧化硫分子含有两个氧原子 | |
| B. | 2N:“2”表示两个氮元素 | |
| C. | $\stackrel{+2}{Mg}$O:“+2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | 2NO3-:“2”表示两个硝酸银离子 |
11.下列归纳和总结完全正确的一组是( )
| A.对除杂的认识 | B.食品安全 |
| ①用稀硫酸除去Zn中混有的Ag ②用灼烧的方法除去Fe2O3中混有的C ③用碳酸钙除去CaCl2溶液中的HCl | ①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③补充维生素A防止夜盲症 |
| C.对现象的认识 | D.化学学科的价值 |
| ①干冰作制冷剂,因为升华时吸收大量的热 ②打开浓盐酸瓶塞,瓶口上方出现大量白烟 ③电解水生成氢气和氧气的体积比为2:1 | ①研制高效低毒农药,保障粮食生产 ②开发新型材料,改善人类生存条件 ③利用化学合成药物,保障人体健康 |
| A. | A | B. | B | C. | C | D. | D |
15.下图所示的四个图象,能正确表示对应关系的是( )
| A. | 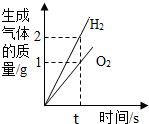 电解水 | |
| B. |  向一定质量锌粒中加入过量稀硫酸 | |
| C. | 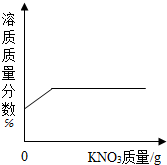 20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 | |
| D. | 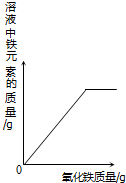 向一定量的稀盐酸中加入足量氧化铁 |
20.下列食物中富含糖类的是( )
| A. | 马铃薯 | B. | 鸡蛋 | C. | 黄瓜 | D. | 花生油 |