题目内容
3.用数字和化学符号填空:(1)2个氢分子2H2
(2)构成氯化钠的微粒Na+、Cl-
(3)氯化亚铁中的阳离子Fe2+
(4)硝酸中氮元素的化合价是+5价H$\stackrel{+5}{N}$O3
(5)乙醇属于可再生燃料,国家正在逐步推广使用乙醇汽油.乙醇的化学式是C2H5OH.
分析 (1)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字进行分析;
(2)根据氯化钠是由钠离子、氯离子构成的进行分析;
(3)根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字进行分析;
(4)根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后进行分析;
(5)根据化学式的正确书写方法进行分析.
解答 解:(1)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个氢分子表示为2H2;
(2)氯化钠是由钠离子、氯离子构成的,化学式为Na+、Cl-;
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,所以氯化亚铁中的阳离子亚铁离子表示为Fe2+;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以硝酸中氮元素的化合价是+5价表示为H$\stackrel{+5}{N}$O3;
(5)乙醇的化学式是C2H5OH.
故答案为:(1)2H2;
(2)Na+、Cl-;
(3)Fe2+;
(4)H$\stackrel{+5}{N}$O3;
(5)C2H5OH.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案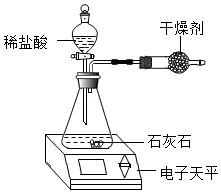
①取研碎后的石灰石2.5克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表,计算出石灰石中碳酸钙的质量分数.
| 反应前总质量(克) | 275.58 |
| 反应后总质量(克) | 274.70 |
| 反应前后质量差(克) | 0.88 |
(2)结合表中数据,计算该石灰石中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑,石灰石中的其它成分不与盐酸反应)
(3)实验后小明认真反思觉得该实验测得的石灰石中碳酸钙的质量分数比实际值会偏小(填“偏大”、“偏小”或“不变”),理由是反应后有部分二氧化碳残留在锥形瓶中使测量得到的二氧化碳的质量变小,故计算得到的碳酸
钙的质量也变小.
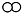 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )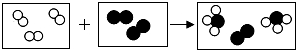
| A. | 在反应过程中A2和B2分子保持不变 | |
| B. | 该反应为置换反应 | |
| C. | 参加反应的A2与B2分子数之比为3:1 | |
| D. | 物质X含4种元素 |
| A. | 原子的电子层数不同 | B. | 原子的中子数不同 | ||
| C. | 原子的质子数不同 | D. | 原子的最外层电子数不同 |
【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液呈碱性,也可能呈酸性,也可能呈中性.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
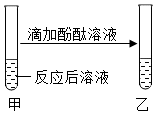 | 无色酚酞溶液变红色; | 溶液呈碱性,使其呈碱性的微粒是氢氧根离子; |
| 无色酚酞溶液不变色 | 溶液呈酸性或中性; |
| 实验操作 | 实验现象 | 实验结论 |
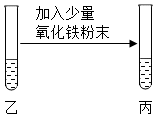 | 粉末部分或全部消失,溶液变为黄色 | 溶液呈酸性,反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O; |
| 无明显变化 | 溶液呈中性; |
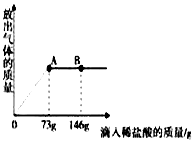 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题:
在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题: 如图是初中化学常见的几种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去).A、B、C、D、E、F分别是两种常见的酸、单质,可榕性钡盐溶液,金属氧化物和非金属氧化物中的一种.用“-”表示两种物质之间可以发生化学
如图是初中化学常见的几种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去).A、B、C、D、E、F分别是两种常见的酸、单质,可榕性钡盐溶液,金属氧化物和非金属氧化物中的一种.用“-”表示两种物质之间可以发生化学