题目内容
12.掌握化学用语是学习化学的关键,请用化学用语填空:(1)①氩元素Ar;②硝酸钾中的阳离子K+;③氯化铝AlCl3;④2个五氧化二磷分子2P2O5.
(2)“Fe2+”中数字“2”表示的意义每个亚铁离子带两个单位的正电荷.
分析 (1)①根据元素符号书写的一大二小原则进行分析;
②根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字进行分析;
③根据化学式的正确书写方法进行分析;
④根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字进行分析;
(2)根据元素符号右上角的数字表示离子所带的电荷数进行分析.
解答 解:(1)①元素符号书写的一大二小原则,所以氩元素表示为Ar;
②离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,所以硝酸钾中的阳离子钾离子表示为K+;
③氯化铝的化学式为AlCl3;
④分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个五氧化二磷分子表示为2P2O5;
(2)元素符号右上角的数字表示离子所带的电荷数,所以“Fe2+”中数字“2”表示的意义是:每个亚铁离子带两个单位的正电荷.
故答案为:(1)Ar;
K+;
AlCl3;
2P2O5;
(2)每个亚铁离子带两个单位的正电荷.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
10.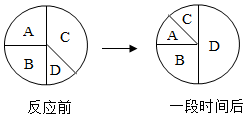 如图表示A、B、C、D四种物质在密闭容器中反应一段时间后质量的变化,则该化学反应的表达式是( )
如图表示A、B、C、D四种物质在密闭容器中反应一段时间后质量的变化,则该化学反应的表达式是( )
 如图表示A、B、C、D四种物质在密闭容器中反应一段时间后质量的变化,则该化学反应的表达式是( )
如图表示A、B、C、D四种物质在密闭容器中反应一段时间后质量的变化,则该化学反应的表达式是( )| A. | A+C→D+B | B. | D→A+C | C. | D$\stackrel{B}{→}$A+C | D. | A+C$\stackrel{B}{→}$ D |
7.下列实验操作错误的是( )
| A. | 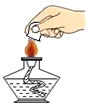 | B. | 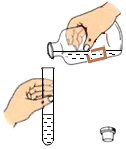 | C. | 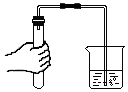 | D. | 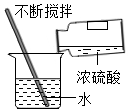 |
4.下列图形能正确反映实验变化关系的是( )
| A. | 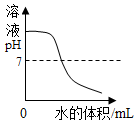 向一定量4%的NaOH溶液中不断加水 | |
| B. | 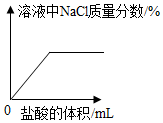 向一定量的NaOH溶液中逐滴加入稀盐酸至过量 | |
| C. | 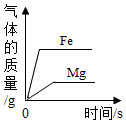 常温下,将等质量的铁和镁分别同时投入足量.等质量分数的稀盐酸中 | |
| D. | 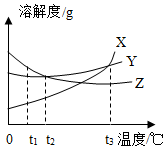 将t3℃时X、Y、Z三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为Y>Z>X |
1.某化学兴趣小组学习碱的性质后,到实验室做实验.小明将二氧化碳通入氢氧化钠溶液后无明显现象,然后向得到的溶液中滴加CaCl2溶液,产生白色沉淀;小杰做的实验和小明一样,但没有出现白色沉淀.他们为了查明原因,查阅资料:①CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CO2+H2O=2NaHCO3;②Ca(HCO3)2溶于水,溶液呈碱性;③CaCl2溶液呈中性:④Na2CO3、NaHCO3溶液都呈碱性,都能与酸反应;⑤铝、锌、铁、铜的盐溶液与NaHCO3溶液混合会产生沉淀.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3;猜想②NaHCO3;猜想③Na2CO3、NaOH;猜想④Na2CO3、NaOH、NaHCO3.
【实验探究】
【继续探究】将4.0gNaOH固体溶解在100mL水中,然后通入4.0g二氧化碳气体,充分反应后,所得溶液的溶质是碳酸钠和碳酸氢钠.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3;猜想②NaHCO3;猜想③Na2CO3、NaOH;猜想④Na2CO3、NaOH、NaHCO3.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| (1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入稀盐酸 | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑. |
| (2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加无色酚酞试液. | 产生白色沉淀;溶液变红. | 猜想③成立 |
2.下列变化中,属于物理变化的是( )
| A. | 胆矾研碎 | B. | 木炭燃烧 | C. | 氢气爆炸 | D. | 钢铁生锈 |