题目内容
13.小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究.【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液呈碱性,也可能呈酸性,也可能呈中性.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
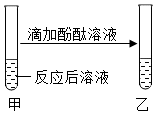 | 无色酚酞溶液变红色; | 溶液呈碱性,使其呈碱性的微粒是氢氧根离子; |
| 无色酚酞溶液不变色 | 溶液呈酸性或中性; |
| 实验操作 | 实验现象 | 实验结论 |
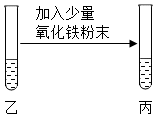 | 粉末部分或全部消失,溶液变为黄色 | 溶液呈酸性,反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O; |
| 无明显变化 | 溶液呈中性; |
分析 【猜想与假设】氢氧化钠溶液与稀盐酸反应生成氯化钠和水,可能恰好完全反应,也可能是稀盐酸有剩余,也可能是氢氧化钠有剩余,进行分析解答.
【实验验证】根据无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,进行分析解答.
【继续验证】根据加入氧化铁后现象为粉末部分或全部消失,溶液变为黄色,结合酸能与氧化铁反应生成盐和水,进行分析解答.
解答 解:【猜想与假设】氢氧化钠溶液与稀盐酸反应生成氯化钠和水,可能恰好完全反应,也可能是稀盐酸有剩余,也可能是氢氧化钠有剩余,故可假设可能呈酸性后中性.
【实验验证】向反应后的溶液中滴加无色酚酞溶液,实验结论是显碱性,则无色酚酞溶液变红色;使其呈碱性的微粒是氢氧根离子.
无色酚酞溶液不变色,说明溶液显酸性或中性.
【继续验证】加入氧化铁后现象为粉末部分或全部消失,溶液变为黄色,是因为盐酸酸能与氧化铁反应生成氯化铁和水,说明溶液呈酸性;反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
若无明显变化,说明溶液显中性.
故答案为:【猜想与假设】酸性;中性;
【实验验证】变红色;氢氧根离子;酸性或中性;
【继续验证】酸性;Fe2O3+6HCl═2FeCl3+3H2O;无明显变化;中性.
点评 本题难度不是很大,掌握酸的化学性质、中和反应的反应原理、化学方程式的书写方法等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
4.下列图形能正确反映实验变化关系的是( )
| A. | 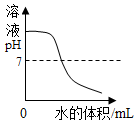 向一定量4%的NaOH溶液中不断加水 | |
| B. | 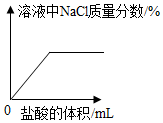 向一定量的NaOH溶液中逐滴加入稀盐酸至过量 | |
| C. | 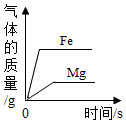 常温下,将等质量的铁和镁分别同时投入足量.等质量分数的稀盐酸中 | |
| D. | 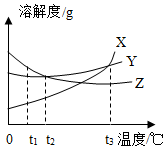 将t3℃时X、Y、Z三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为Y>Z>X |
1.某化学兴趣小组学习碱的性质后,到实验室做实验.小明将二氧化碳通入氢氧化钠溶液后无明显现象,然后向得到的溶液中滴加CaCl2溶液,产生白色沉淀;小杰做的实验和小明一样,但没有出现白色沉淀.他们为了查明原因,查阅资料:①CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CO2+H2O=2NaHCO3;②Ca(HCO3)2溶于水,溶液呈碱性;③CaCl2溶液呈中性:④Na2CO3、NaHCO3溶液都呈碱性,都能与酸反应;⑤铝、锌、铁、铜的盐溶液与NaHCO3溶液混合会产生沉淀.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3;猜想②NaHCO3;猜想③Na2CO3、NaOH;猜想④Na2CO3、NaOH、NaHCO3.
【实验探究】
【继续探究】将4.0gNaOH固体溶解在100mL水中,然后通入4.0g二氧化碳气体,充分反应后,所得溶液的溶质是碳酸钠和碳酸氢钠.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3;猜想②NaHCO3;猜想③Na2CO3、NaOH;猜想④Na2CO3、NaOH、NaHCO3.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| (1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入稀盐酸 | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑. |
| (2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加无色酚酞试液. | 产生白色沉淀;溶液变红. | 猜想③成立 |
5.下列实验现象描述,完全正确的是( )
| A. | 细铁丝在氧气中剧然燃烧,火星四射,生成黑色四氧化三铁 | |
| B. | 硫在氧气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体 | |
| C. | 木炭在空气中燃烧发出红光,在氧气中燃烧发出白光 | |
| D. | 打开盛放浓硫酸试剂瓶的瓶盖,瓶口出现白雾 |
2.下列变化中,属于物理变化的是( )
| A. | 胆矾研碎 | B. | 木炭燃烧 | C. | 氢气爆炸 | D. | 钢铁生锈 |
2.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展.流程简图如图所示(已知:母液中有一种铵态氮肥),下列有关说法不正确的是( )


| A. | 反应中先通入氨气的目的是促进二氧化碳的吸收,提高产率 | |
| B. | 流程中“某操作”用到的玻璃仪器有:玻璃棒、烧杯、量筒 | |
| C. | 反应II得到的CO2可以循环使用 | |
| D. | 反应I的方程式为NaCl+NH3+CO2═NaHCO3↓+NH4Cl |

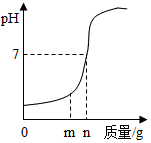 用氢氧化钠中和一定量的盐酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示:
用氢氧化钠中和一定量的盐酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示: