题目内容
3.能共存于pH=13且溶液颜色为无色透明的溶液的离子组是( )| A. | H+ Cl- NO3- Ba2+ | B. | Na+ Cu2+ Cl- NO3- | ||
| C. | Fe3+ K+ Cl- SO42- | D. | Ba2+ NO3- Na+ Cl- |
分析 pH为13的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应发生的条件可知,复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存;本题还要注意溶液呈无色透明,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为13的水溶液显碱性,水溶液中含有大量的OH-.
A、H+与碱性溶液中的OH-两种离子能结合成水,不能大量共存,故选项错误;
B、Cu2+与碱性溶液中的OH-两种离子能结合成氢氧化铜沉淀,不能大量共存,且Cu2+的水溶液蓝色,故选项错误;
C、Fe3+与碱性溶液中的OH-两种离子能结合成氢氧化铁沉淀,不能大量共存,且Fe3+的水溶液黄色,故选项错误;
D、四种离子间不能结合成沉淀、气体或水,能大量共存,且不存在有色离子,故选项正确.
故选:D.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在碱性溶液中共存及特定离子的颜色.

练习册系列答案
相关题目
18.现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液.为了测定碱性调味液中碳酸钠的质量分数,某同学进行了如下实验:取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某浓度的稀硫酸中,测得三组实验数据见下表(气体的溶解忽略不计):
根据实验及有关数据进行计算:
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为5.5g.
(2)碱性调味液中碳酸钠的质量分数为多少?
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀硫酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/s | 2.2 | 4.4 | 5.5 |
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为5.5g.
(2)碱性调味液中碳酸钠的质量分数为多少?
8.用下列方法鉴别物质不能达到实验目的是( )
| 序号 | 实验目的 | 试剂或方法 |
| A | 鉴别FeCl3、NaCl、NaOH、MgCl2四种溶液 | 不另加试剂 |
| B | 鉴别CaCO3、NaCl、NaOH、NH4NO3四种固体粉末 | 水 |
| C | Na2SO4溶液与AgNO3溶液 | 分别加入BaCl2溶液 |
| D | 除去氮气中的少量氧气 | 通过灼热的铜网 |
| A. | A | B. | B | C. | C | D. | D |
15.空气是一种宝贵的资源,空气中可用作保护气和制造多种用途电光源的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
17.随着人们的生活水平逐年调高对饮用水的健康问题十分关注,如图为某品牌矿泉水标签的部分内容,请用恰当的化学用语填空:
(1)说明书上所涉及到的“钾、镁”是指化学上的元素;
(2)写出其中的一种阳离子K+;
(3)标出水中氧元素的化合价H2$\stackrel{-2}{O}$;
(4)图1是镁(Mg)原子的构成示意图,根据图示信息回答下列问题:
①在化学反应中镁原子容易失去(“得到”或“失去”)电子:形成离子符号表示为Mg2+.
②镁原子与下列如图2元素化学性质相似的是A;

(5)写出由上述离子构成的硫酸盐的化学式MgSO4(任写一种).
| 健康饮水新概念 饮水质量好坏对人体健康至关重要,矿物质水含钾、镁等游离态矿物质,补充人体所需,让身体保持健康与活力.喝的健康,生活更健康! 主要成分:钾离子:1.0-27.0mg/L 氯离子:1.0-24.0mg/L镁离子:0.1-5.0mg/L 硫酸根离子:0.4-20.0mg/L |
(2)写出其中的一种阳离子K+;
(3)标出水中氧元素的化合价H2$\stackrel{-2}{O}$;
(4)图1是镁(Mg)原子的构成示意图,根据图示信息回答下列问题:
①在化学反应中镁原子容易失去(“得到”或“失去”)电子:形成离子符号表示为Mg2+.
②镁原子与下列如图2元素化学性质相似的是A;

(5)写出由上述离子构成的硫酸盐的化学式MgSO4(任写一种).
 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示: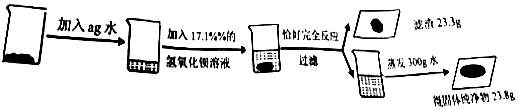
 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线.
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线.