题目内容
5.金属与人类生活密切相关.请分析回答下列问题:(1)人体中含量最高的金属元素是钙
(2)铝制品具有很好的抗腐蚀性能,其原因是(用化学方程式表示)4Al+3O2=2Al2O3;
(3)往AgN03溶液中加入一定量锌和铜的混合粉末,充分反应后,过滤,滤液为蓝色,则滤液中含有的金属离子是Zn2+、Cu2+,Zn2+、Cu2+、Ag+(写出所有存在的可能组合)
分析 (1)根据人体中含量最高的金属元素是钙进行分析;
(2)根据铝和氧气反应生成氧化铝进行分析;
(3)根据锌比铜活泼,铜比银活泼进行分析.
解答 解:(1)人体中含量最高的金属元素是钙;
(2)铝和氧气反应生成氧化铝,化学方程式为:4Al+3O2=2Al2O3;
(3)往AgNO3溶液中加入一定量锌和铜的混合粉末,锌先和硝酸银反应生成硝酸锌和银,锌完全反应后,铜再和硝酸银反应生成硝酸铜和银,充分反应后,过滤,滤液为蓝色,说明铜参加了反应,如果硝酸银完全反应,则滤液中含有硝酸锌和硝酸铜,如果硝酸银过量,则滤液中含有硝酸锌、硝酸铜和硝酸银,则滤液中含有的溶质可能是硝酸锌、硝酸铜,或硝酸锌、硝酸铜、硝酸银,所以滤液中含有的金属离子是Zn2+、Cu2+,Zn2+、Cu2+、Ag+.
故答案为:(1)钙;
(2)4Al+3O2=2Al2O3;
(3)Zn2+、Cu2+,Zn2+、Cu2+、Ag+.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
20.氢氧化钠是一种重要的化工原料,也是实验室中常见的一种试剂,氢氧化钠必须密封保存,用化学方程式表示变质原因2NaOH+CO2═Na2CO3+H2O.
探究一:确定一瓶氢氧化钠固体是否变质
探究二:确定氢氧化钠固体变质的程度
实验方案中滴入过量的CaCl2溶液目的是除尽碳酸钠.
探究一:确定一瓶氢氧化钠固体是否变质
| 实验操作 | 实验现象 | 结论 |
| 取少量样品于试管中,加入适量水,样品全溶解后,滴加足量的稀盐酸(填一种溶液名称) | 有气泡产生 | 氢氧化钠固体已变质 |
| 实验操作 | 实验现象 | 结论 |
| ①取少量样品于试管中,加入适量水,样品全溶解后,滴加过量的CaCl2溶液 | 产生白色沉淀 | 氢氧化钠固体部分变质 |
| ②静置后取上层清液于试管中,滴入2滴酚酞试液 | 溶液变为红色 |
17.PM2.5是指大气中直径不超过2.5μm的颗粒物,主要来源是化石燃料的燃烧和扬尘.它是造成雾霾天气的元凶之一,吸入人体后能直接进入支气管,因而对人体健康影响更大.下列措施能减少PM2.5污染的是( )
| A. | 鼓励焚烧秸秆节约能源 | B. | 鼓励燃煤火力发电 | ||
| C. | 鼓励使用太阳能热水器 | D. | 鼓励开私家车出行 |
15.下列各组物质的溶液,不另加试剂则无法鉴别的是( )
| A. | NaOH、HCl、CuSO4、MgSO4 | B. | KNO3、HCl、NaCl、NaOH | ||
| C. | Na2CO3、K2SO4、BaCl2、HCl | D. | 酚酞、H2SO4、NaOH、MgCl2 |
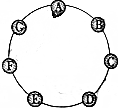

 A~F均为初中常见的化学物质(“→“表示物质间的转化关系,“-”表示两端的物质能发生化学反应).其中A、E是常见的两种氧化物;B、C是常见的两种碱;D、F是常见的两种盐.它们之间有如右图的相互转化关系(图中部分生成物已略去).请问答下列间题:
A~F均为初中常见的化学物质(“→“表示物质间的转化关系,“-”表示两端的物质能发生化学反应).其中A、E是常见的两种氧化物;B、C是常见的两种碱;D、F是常见的两种盐.它们之间有如右图的相互转化关系(图中部分生成物已略去).请问答下列间题: