题目内容
8.如图A~G七种物质按如图方式排列,连线两端的物质可以发生反应.已知七种物质分别是如下八种物质中的一种:碳、氧气、铁、二氧化碳、水、稀盐酸、纯碱、熟石灰.如果A是空气中性质较活泼的成分,B是金属单质,E和F发生的反应不属于基本反应类型.请回答下列问题.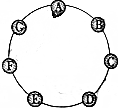
(1)写出E的化学式Ca(OH)2.
(2)用化学方程式表示C、D间的反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)图中所示反应中没有涉及的基本反应类型是分解反应.
(4)下列物质可替换D的是K2CO3.
分析 空气中性质较活泼的成分是氧气,点燃条件下,氧气能和金属单质铁反应生成四氧化三铁,铁能和稀盐酸反应生成氯化亚铁和氢气,稀盐酸能和碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水,不属于基本反应类型,高温条件下,二氧化碳能和碳反应生成一氧化碳,点燃条件下,碳能和氧气反应生成二氧化碳.
解答 解:空气中性质较活泼的成分是氧气,点燃条件下,氧气能和金属单质铁反应生成四氧化三铁,铁能和稀盐酸反应生成氯化亚铁和氢气,稀盐酸能和碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水,不属于基本反应类型,高温条件下,二氧化碳能和碳反应生成一氧化碳,点燃条件下,碳能和氧气反应生成二氧化碳,因此A~G七种物质分别是氧气、铁、稀盐酸、碳酸钠、氢氧化钙、二氧化碳、碳;
(1)E是氢氧化钙,氢氧化钙的化学式是Ca(OH)2.
故填:Ca(OH)2.
(2)稀盐酸能和碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)图中所示反应中,铁和氧气反应属于化合反应,铁和稀盐酸反应属于置换反应,稀盐酸和碳酸钠反应属于复分解反应,没有涉及的基本反应类型是分解反应.
故填:分解.
(4)碳酸钾能和稀盐酸反应生成氯化钾、水和氧气,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾,因此碳酸钾可以代替碳酸钠.
故填:K2CO3.
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.

| A. | 甲状腺机能亢进患者要食用低钠盐 | B. | 食用加铁酱油防止贫血 | ||
| C. | 骨质疏松患者日常可食用高钙牛奶 | D. | 使用含氟牙膏预防龋齿 |
| 物质 | X | Y | Z | Q |
| 第一次测得的质量/g | 68 | 16 | 4.4 | 3.6 |
| 第二次测得的质量/g | 4 | 未测 | 48.4 | 39.6 |
| A. | 该反应一定是复分解反应 | B. | 若X为氧气,则Y一定发生氧化反应 | ||
| C. | 第二次测定时,Y已完全反应 | D. | 该反应中Z与Q质量变化之比为11:9 |
 a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | 15℃时,a、b的溶液溶质质量分数相等 | |
| B. | 加水或升温均可使a、b的饱和溶液变为不饱和溶液 | |
| C. | 将15℃时b的饱和溶液升温至30℃,溶质质量分数不变 | |
| D. | 15℃时分别向100 g水中加入20 g a和b,降温至0℃,所得溶液均为饱和溶液 |

【提出问题】分组实验中,出现意想不到现象的原因是什么呢?
【猜想与假设】
I.石灰水未变浑浊,是因为二氧化碳中混有少量氯化氢气体.
Ⅱ.石灰水未变浑浊,是因为石灰水的浓度过小(或通入二氧化碳的时间过短).
Ⅲ.石灰水出现浑浊后又变澄清,与石灰水的浓度、通入二氧化碳的时间有关.
【进行实验】实验装置如图2所示.
提示:①实验中所用盐酸与分组实验所用盐酸相同;
②CO2在饱和NaHCO3溶液中的溶解度非常小.
步骤1:分别取一定体积的饱和澄清石灰水与一定体积的蒸馏水混合配制成50mL溶液.
步骤2:分别向50mL溶液中通入一段时间的二氧化碳,记录现象.
| 实验序号 | V饱和石灰水/mL | V蒸馏水 /mL | 出现现象所需时间/s | |||
| 开始浑浊 | 明显浑浊 | 沉淀减少 | 是否澄清 | |||
| ① | 50 | 0 | 19 | 56 | 366 | 持续通入CO28min以上,沉淀不能完全消失 |
| ② | 40 | 10 | 24 | 51 | 245 | |
| ③ | 30 | 20 | 25 | 44 | 128 | |
| ④ | 20 | 30 | 27 | 35 | 67 | 89s后完全澄清 |
| ⑤ | 10 | 40 | 通3min以上,均无明显现象 | |||
(1)实验中,所用石灰水为饱和溶液的是①(填序号).
(2)二氧化碳使澄清石灰水变浑浊原因是Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
(3)饱和NaHCO3溶液的作用是除去氯化氢气体.
(4)通过实验分析,猜想 I不成立(填“成立”或“不成立”),猜想Ⅱ、Ⅲ成立.
【反思与评价】
(5)向澄清的石灰水中通入二氧化碳,为避免出现“意想不到的现象”,你的建议是所用石灰水的浓度不能太小(或用饱和的石灰水),通入二氧化碳的时间不能过短也不能过长.

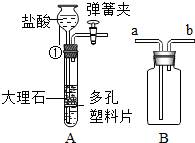 根据如图回答问题.
根据如图回答问题.