题目内容
某班一学习小组以“关于市场上几种补钙保健产品的调查研究”为课题进行了探究学习活动.请你一起参与其活动,完成下列探究过程.
【调查收集资料】
通过市场调查,常见的四种钙产品的有关信息如下:
【交流与讨论】
①由上表分析比较,四种钙产品中,当含有相同质量的钙元素时 价格相对最便宜.
A.钙尔奇-DB.凯思立-DC.乐力钙D.枸橼酸钙
②在交流过程中,小芳同学提出一个观点,补钙还可以食补,即能省钱又能补钙.下列做法可以补钙的是 .
A.在食物中添加生石灰 B.食用一些虾皮 C.喝排骨汤D.做馒头时放纯碱
③小明认为食用凯思立-D的碳酸钙进入胃内能发生化学反应,其化学方程式是: .
【质疑与再探究】
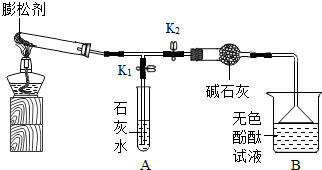
钙尔奇-D说明书上标注每片钙尔奇-D中含碳酸钙1.5g.(已知:钙尔奇-D不含有其他碳酸盐,其研细后能与稀硫酸完全反应.)在讨论中,小强同学提出一个问题,现在市场上有些不法分子会以假乱真,购买的钙尔奇-D不知是否合格,想通过实际定量分析.小强设计了如下方案并进行实验:取5片钙尔奇-D研细,放入锥形瓶(见图),加入足量的盐酸充分反应,气体最后通入氢氧化钠溶液(假设气体全部被氢氧化钠吸收,忽略系统内空气中CO2的影响),两次称量盛氢氧化钠溶液的洗气瓶来确定产生二氧化碳质量,再通过计算可判断出样品是否合格.试回答下列问题:

①小强用B中NaHCO3饱和溶液除去CO2中混有的少量HCl气体,B中的NaHCO3溶液能否换成石灰水? (填“能”或“否”),其理由是 .(用化学方程式表示)
②C装置的作用是
③小明认为:小强的设计不能达到检验样品是否合格的目的,应该加以改进,并得到了小组其他同学的赞同.其改进的方法是 .
④用改进后的装置和药品进行实验,称量盛氢氧化钠溶液的洗气瓶增加了3.3g,试通过计算小强选用的钙尔奇-D (选填“是”或“不是”)合格产品.
【调查收集资料】
通过市场调查,常见的四种钙产品的有关信息如下:
| 品名 | 钙尔奇-D | 凯思立-D | 乐力钙 | 枸橼酸钙 |
| 主要含钙物质 | 碳酸钙 | 碳酸钙 | 氨基酸螯合钙 | 枸橼酸钙 |
| 钙元素含量(mg/片) | 600 | 500 | 250 | 168 |
| 数量(片)/瓶(盒) | 30 | 20 | 30 | 30 |
| 价格(元)/瓶(盒) | 27.00 | 23.10 | 30.00 | 25.20 |
①由上表分析比较,四种钙产品中,当含有相同质量的钙元素时
A.钙尔奇-DB.凯思立-DC.乐力钙D.枸橼酸钙
②在交流过程中,小芳同学提出一个观点,补钙还可以食补,即能省钱又能补钙.下列做法可以补钙的是
A.在食物中添加生石灰 B.食用一些虾皮 C.喝排骨汤D.做馒头时放纯碱
③小明认为食用凯思立-D的碳酸钙进入胃内能发生化学反应,其化学方程式是:
【质疑与再探究】
钙尔奇-D说明书上标注每片钙尔奇-D中含碳酸钙1.5g.(已知:钙尔奇-D不含有其他碳酸盐,其研细后能与稀硫酸完全反应.)在讨论中,小强同学提出一个问题,现在市场上有些不法分子会以假乱真,购买的钙尔奇-D不知是否合格,想通过实际定量分析.小强设计了如下方案并进行实验:取5片钙尔奇-D研细,放入锥形瓶(见图),加入足量的盐酸充分反应,气体最后通入氢氧化钠溶液(假设气体全部被氢氧化钠吸收,忽略系统内空气中CO2的影响),两次称量盛氢氧化钠溶液的洗气瓶来确定产生二氧化碳质量,再通过计算可判断出样品是否合格.试回答下列问题:

①小强用B中NaHCO3饱和溶液除去CO2中混有的少量HCl气体,B中的NaHCO3溶液能否换成石灰水?
②C装置的作用是
③小明认为:小强的设计不能达到检验样品是否合格的目的,应该加以改进,并得到了小组其他同学的赞同.其改进的方法是
④用改进后的装置和药品进行实验,称量盛氢氧化钠溶液的洗气瓶增加了3.3g,试通过计算小强选用的钙尔奇-D
考点:实验探究物质的组成成分以及含量,气体的净化(除杂),盐的化学性质,化合物中某元素的质量计算,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算,人体的元素组成与元素对人体健康的重要作用
专题:科学探究
分析:[交流与讨论]
(1)根据各种药品的主要成分中含有钙元素的质量和其价格比比较回答;
(2)根据钙元素的主要食物来源回答;
(3)根据胃酸的成分与它和碳酸钙的化学性质回答.
[质疑与再探究]
(1)根据二氧化碳和NaHCO3饱和溶液的化学性质回答;
(2)根据碳酸氢钠和盐酸反应生成了二氧化碳的情况回答;
(3)根据浓硫酸的作用回答;
(4)根据盛氢氧化钠溶液的洗气瓶增加了3.3 g,判断生成的二氧化碳的质量,再根据二氧化碳的质量求出碳酸钙的质量,最后判断是否合格.
(1)根据各种药品的主要成分中含有钙元素的质量和其价格比比较回答;
(2)根据钙元素的主要食物来源回答;
(3)根据胃酸的成分与它和碳酸钙的化学性质回答.
[质疑与再探究]
(1)根据二氧化碳和NaHCO3饱和溶液的化学性质回答;
(2)根据碳酸氢钠和盐酸反应生成了二氧化碳的情况回答;
(3)根据浓硫酸的作用回答;
(4)根据盛氢氧化钠溶液的洗气瓶增加了3.3 g,判断生成的二氧化碳的质量,再根据二氧化碳的质量求出碳酸钙的质量,最后判断是否合格.
解答:解:
[交流与讨论]
①600mg/片×30片÷27.00元=666.67 mg/元;500mg/片×20片÷23.10元=432.9 mg/元;250mg/片×30片÷30.00元=250 mg/元;168mg/片×30片÷25.20元=200 mg/元,所以选A.
②A.在食物中添加生石灰,生石灰会腐蚀人的消化道;B.食用一些虾皮可以,虾皮中富含钙;C.喝排骨汤可以,骨头汤中含钙元素多;D.做馒头时放纯碱不可以,纯碱是碳酸钠,不含钙元素;所以选BC.
③胃酸的主要成分是盐酸,它和碳酸钙反应生成氯化钙、水和二氧化碳,方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
[质疑与再探究]
①B中的NaHCO3溶液不能换成石灰水,因为石灰水的主要成分是氢氧化钙,能和二氧化碳也发生反应,反应的化学方程式是:Ca(OH)2+CO2=CaCO3↓+H2O
②C装置的作用是干燥CO2气体;
③小明认为:小强的设计不能达到检验样品是否合格的目的,NaHCO3饱和溶液吸收HCl时,要反应产生CO2,导致盛NaOH溶液的洗气瓶增重大于样品产生CO2的质量,无法计算样品是否合格,应该加以改进,其改进的方法是:将盐酸换成稀硫酸,就不会有氯化氢气体挥发出来,再将NaHCO3饱和溶液的洗气瓶去掉就可以了.
④设钙尔奇-D是碳酸钙的质量为X
由于盛氢氧化钠溶液的洗气瓶增加了3.3 g,则生成的二氧化碳的质量3.3 g.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 3.3g
100÷44=X÷3.3g X=7.5g
7.5g÷5片=1.5g/片 与说明书一致,为合格产品.
故答案为:
[交流与议论]
①A;
②BC;
③CaCO3+2HCl=CaCl2+H2O+CO2↑;
[质疑与再探究]
①否;因为石灰水也能吸收二氧化碳;
②干燥CO2气体;
③将盐酸换成稀硫酸,将NaHCO3饱和溶液的洗气瓶去掉;
④是.
[交流与讨论]
①600mg/片×30片÷27.00元=666.67 mg/元;500mg/片×20片÷23.10元=432.9 mg/元;250mg/片×30片÷30.00元=250 mg/元;168mg/片×30片÷25.20元=200 mg/元,所以选A.
②A.在食物中添加生石灰,生石灰会腐蚀人的消化道;B.食用一些虾皮可以,虾皮中富含钙;C.喝排骨汤可以,骨头汤中含钙元素多;D.做馒头时放纯碱不可以,纯碱是碳酸钠,不含钙元素;所以选BC.
③胃酸的主要成分是盐酸,它和碳酸钙反应生成氯化钙、水和二氧化碳,方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
[质疑与再探究]
①B中的NaHCO3溶液不能换成石灰水,因为石灰水的主要成分是氢氧化钙,能和二氧化碳也发生反应,反应的化学方程式是:Ca(OH)2+CO2=CaCO3↓+H2O
②C装置的作用是干燥CO2气体;
③小明认为:小强的设计不能达到检验样品是否合格的目的,NaHCO3饱和溶液吸收HCl时,要反应产生CO2,导致盛NaOH溶液的洗气瓶增重大于样品产生CO2的质量,无法计算样品是否合格,应该加以改进,其改进的方法是:将盐酸换成稀硫酸,就不会有氯化氢气体挥发出来,再将NaHCO3饱和溶液的洗气瓶去掉就可以了.
④设钙尔奇-D是碳酸钙的质量为X
由于盛氢氧化钠溶液的洗气瓶增加了3.3 g,则生成的二氧化碳的质量3.3 g.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 3.3g
100÷44=X÷3.3g X=7.5g
7.5g÷5片=1.5g/片 与说明书一致,为合格产品.
故答案为:
[交流与议论]
①A;
②BC;
③CaCO3+2HCl=CaCl2+H2O+CO2↑;
[质疑与再探究]
①否;因为石灰水也能吸收二氧化碳;
②干燥CO2气体;
③将盐酸换成稀硫酸,将NaHCO3饱和溶液的洗气瓶去掉;
④是.
点评:化学来源于生产、生活,也必须服务于生产、生活,所以与生产、生活有关的化学知识考查必是热点之一.

练习册系列答案
相关题目
H2,CO,CO2,CH4四种气体,从物质分类上有别于其他三种的是( )
| A、CH4 |
| B、CO |
| C、CO2 |
| D、H2 |
下列实验操作中,正确的是( )
A、 点燃酒精灯 |
B、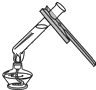 液体加热 |
C、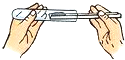 固体粉末取用 |
D、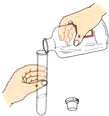 液体倾倒 |
下列实验操作中,能达到预期目的是( )
| A、用紫色石蕊试液检测某溶液的酸碱度 |
| B、用10mL水和10mL酒精配制成20mL酒精溶液 |
| C、用100毫升的量筒量取55毫升的稀硫酸 |
| D、用排水法收集一瓶较纯氧气,导管口有气泡,立即收集 |