题目内容
4. (1)如图将CO2倒入放有高低不同蜡烛的烧杯中,产生的现象是下层蜡烛先熄灭,上层蜡烛后熄灭,说明了①二氧化碳密度比空气大;②不燃烧、不支持燃烧.由这两个性质决定了二氧化碳的用途能灭火.
(1)如图将CO2倒入放有高低不同蜡烛的烧杯中,产生的现象是下层蜡烛先熄灭,上层蜡烛后熄灭,说明了①二氧化碳密度比空气大;②不燃烧、不支持燃烧.由这两个性质决定了二氧化碳的用途能灭火.(2)二氧化碳能灭火的原因是二氧化碳不燃烧、不支持燃烧且密度比空气大.
分析 依据实验现象分析二氧化碳的性质,并据其性质确定其用途.
解答 解:根据题意,由图可知:向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳不燃烧、不支持燃烧且密度比空气大,据此性质,二氧化碳可用于灭火.
故答案为:(1)下层蜡烛先熄灭,上层蜡烛后熄灭;①二氧化碳密度比空气大;②不燃烧、不支持燃烧;灭火;(2)二氧化碳不燃烧、不支持燃烧且密度比空气大.
点评 此题考查知识点的方式比较灵活,但并不是难题,同学们只要掌握二氧化碳的物理化学性质就可以顺利完成该题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.做馒头时在发酵的面团中加入某种物质,既能除去面团中的酸又能使馒头变软,则加入的这种物质为( )
| A. | 氢氧化钠 | B. | 碳酸钠 | C. | 氧化钙 | D. | 氯化钠 |
9.酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图1所示相关的实验.下面是两个小组的实验
记录与分析.请根据要求回答问题:
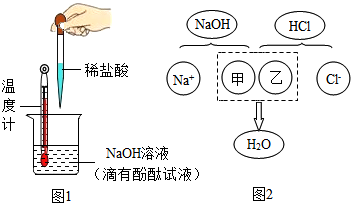
(1)甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸(室温下),反应中溶液温度的变化记录如下:
根据上表数据分析:
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是中和反应放热,恰好完全反应时放出热量最多.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠和氢氧化钠.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.图2描述的是氢氧化钠与盐酸反应的微观实质,请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
(2)请你参与完成乙组同学的实验记录与分析.
记录与分析.请根据要求回答问题:

(1)甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸(室温下),反应中溶液温度的变化记录如下:
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升 (△t)/℃ | 5.6 | 9.8 | 12.1 | 16.3 | 18.5 | 17.1 | 15.2 | 14.6 | 13.5 | 12.6 |
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是中和反应放热,恰好完全反应时放出热量最多.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠和氢氧化钠.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.图2描述的是氢氧化钠与盐酸反应的微观实质,请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
(2)请你参与完成乙组同学的实验记录与分析.
| 实验操作 | 实验现象 | 分析与结论 |
| 步骤一:往装有氢氧化钠溶液样品的试管中先滴加2~3滴的 酚酞试液,再逐滴加入稀盐酸 | 现象一:有气泡产生 现象二:溶液由红色逐渐变成无色 | 1.该氢氧化钠溶液样品已变质 2.溶液碱性消失 |
| 步骤二:取步骤一反应后的溶液,然后逐滴加入该氢氧化钠溶液样品 | 现象一:有气泡产生 现象二:溶液开始不变色,后逐渐变成红色 | 1.产生“气泡”这一现象对应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ 2.所取的步骤一反应后的溶液pH<7(填“<”、“=”或“>”) |
12.下列有关说法中正确的是( )
| A. | 可以用肥皂水来鉴别硬水和软水 | |
| B. | 锅内食用油着火,常用锅盖盖灭,其灭火的原理是清除可燃物 | |
| C. | 过滤、蒸馏、煮沸等操作都可以把硬水变成软水 | |
| D. | 人类利用的能量都是通过化学反应获得的 |
19.废旧计算机的某些部件里含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,将它收集并与足量的稀盐酸充分反应后,过滤,剩余固体中不含有的金属是( )
| A. | Cu、Ag | B. | Zn、Fe | C. | Pt、Cu | D. | Ag、Au |
9.化学实验中常常出现“1+1=2”或“1+1≠2”的有趣现象.下列符合“1+1=2”的事实是( )
| A. | 常温下,1L水与1L酒精混合后的体积等于2L | |
| B. | 室温下,1g镁与1g稀硫酸充分反应后所得的溶液质量为2g | |
| C. | 20℃,1g氯化钠饱和溶液中加入1g氯化钠固体能得到2g氯化钠溶液 | |
| D. | 室温下,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 |
16.下列说法正确的是( )
| A. | 加入催化剂,化学反应一定加快 | |
| B. | 不使用催化剂,化学反应不能进行 | |
| C. | 使用催化剂,可以增加生成物的质量 | |
| D. | 使用催化剂,可以改变化学反应的速率 |

