题目内容
5. 图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.
图中,A代表地壳中含量第二位的金属,C为黑色粉末,E在常温下为液态且为相对分子质量最小的氧化物.常温下,相连环物质间能发生反应,请填空.(1)写出下列物质的化学式:AFeBO2CCDCO2EH2O.
(2)写出各相连环物质间发生的反应
A+B3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
B+CC+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
C+DCO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
D+ECO2+H2O=H2CO3.
分析 根据A代表地壳中含量第二位的金属,所以A是铁,E在常温下为液态且为相对分子质量最小的氧化物,所以E是水,常温下,相连环物质间能发生反应,C为黑色粉末,B会与A、C反应,所以C是碳,B是氧气,D会与二氧化碳和碳反应,所以D是二氧化碳,然后将推出的各种物质进行验证即可.
解答 解:(1)A代表地壳中含量第二位的金属,所以A是铁,E在常温下为液态且为相对分子质量最小的氧化物,所以E是水,常温下,相连环物质间能发生反应,C为黑色粉末,B会与A、C反应,所以C是碳,B是氧气,D会与二氧化碳和碳反应,所以D是二氧化碳,铁和氧气反应生成四氧化三铁,氧气和碳反应生成二氧化碳,碳与二氧化碳反应生成一氧化碳,二氧化碳和水会生成碳酸,推导正确,所以A是Fe,B是O2,C是C,D是CO2,E是H2O;
(2)A+B的反应是铁和氧气在点燃的条件下反应生成四氧化三铁,化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
B+C的反应是碳和氧气在点燃的条件下生成二氧化碳,化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
C+D的反应是二氧化碳和碳在高温的条件下生成一氧化碳,化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
D+E的反应是二氧化碳和水反应生成碳酸,化学方程式为:CO2+H2O=H2CO3.
故答案为:(1)Fe,O2,C,CO2,H2O;
(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,CO2+H2O=H2CO3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 给试管里的液体加热时,试管口对着没有人的方向 | |
| B. | 用胶头滴管向试管中滴加液体时,把滴管伸入试管内 | |
| C. | 在实验室里制取氢气,先检查装置的气密性 | |
| D. | 浓硫酸沾到皮肤上,要立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液 |
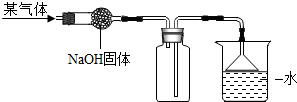
| 气体性质\序号 | A | B | C | D |
| 溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
| 其密度(ρ1)与空气密度(ρ2)比较 | ρ1>ρ2 | ρ1>ρ2 | ρ1<ρ2 | ρ2<ρ1 |
| 在水中的溶解度 | 极易溶 | 难溶 | 极易溶 | 难溶 |
| A. | A | B. | B | C. | C | D. | D |
有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
(2)求12g克该石灰石中碳酸钙的质量是多少克?
(3)该石灰石中碳酸钙的质量分数为83.3%(结果保留一位小数)
| 物质 | A | B | C | D |  |
| 分子示意图 | ? |  |  |  |
(2)物质A中各元素的质量比为碳、氢元素的质量比为9:2.
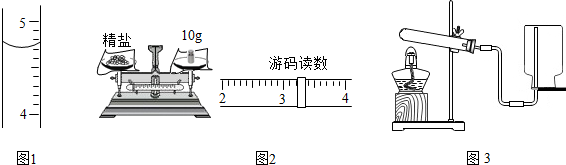

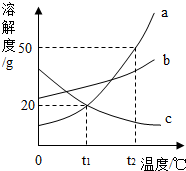 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述中正确的是B.
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述中正确的是B.