题目内容
14.为了对氯化钾样品(含KNO3)进行分析,甲、乙、丙三位同学分别进行实验.他们的实验数据如下表,请仔细观察和分析数据,回答下列问题:| 项目 | 甲 | 乙 | 丙 |
| 所取固体样品质量(克) | 20 | 10 | 10 |
| 加入AgNO3溶液的质量(克) | 100 | 100 | 200 |
| 反应后所得的沉淀质量(克) | 14.35 | 14.35 | 14.35 |
(2)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的滤液中只含有一种溶质?此溶液的溶质质量分数是多少?
分析 (1)由生成沉淀的质量根据硝酸银与氯化钾反应的化学方程式可以计算出样品中氯化钾的质量和生成硝酸钾的质量,进而计算出样品中氯化钾的质量分数.
(2)只有恰好完全反应时,所得溶液中的溶质和原固体中所含的杂质才是同一种物质.所得溶液中溶质的质量由生成的硝酸钾和固体中含有的硝酸钾两部分组成;所得溶液的质量为固体质量与硝酸银溶液的质量和去掉生成沉淀的质量.根据溶质质量分数的计算公式可以计算出所得溶液中溶质的质量分数.
解答 解:甲、乙两组数据对照,说明甲中固体过量,硝酸银溶液完全反应;乙、丙两组数据对照,说明丙中硝酸银溶液过量,固体完全反应;以上分析说明乙中固体与硝酸银溶液恰好完全反应.计算时应以乙组数据为准.
(1)设样品中氯化钾的质量分数为x,生成硝酸钾的质量为y.
KCl+AgNO3=AgCl↓+KNO3
74.5 143.5 101
10g×x 14.35g y
$\frac{74.5}{10g×x}=\frac{143.5}{14.35g}=\frac{101}{y}$
x=74.50%,y=10.1g
(2)所得溶液中溶质的质量分数为$\frac{10g×(1-74.5%)+10.1g}{10g+100g-14.35g}$×100%≈13.23%
答:(1)样品中氯化钾的质量分数为74.50%;
(2)乙;所得溶液中溶质的质量分数为13.23%.
点评 本题主要考查有关含杂质物质的化学方程式计算,难度较大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
9.人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此.下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是( )
| A. | 有酸味的物质 | B. | 一切酸中都含有氧 | ||
| C. | 只有氢才是酸不可缺少的元素 | D. | 与碱作用时失去原有性质的物质 |
19.现有一组物质:海水、盐酸、酒精溶液,下列物质中,可以和这组物质归为同一类的是( )
| A. | 冰水 | B. | 泥水 | C. | 氨水 | D. | 原油 |
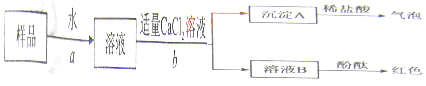
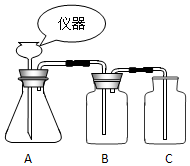 根据如图装置回答下列问题:
根据如图装置回答下列问题:


