题目内容
3.80克溶质的质量分数为10%的氯化钾溶液中,溶质的质量为8 g,溶剂的质量为72 g.(1)一变:若向原溶液中加入40g水,则所得溶液的溶质质量分数为6.7%(计算结果精确到0.1%)
(2)二变:若向原溶液中加入20g氯化钾固体(固体全部溶解),则所得溶液的溶质质量分数为28%
(3)三变:若使原溶液的溶质质量分数变为5%,则应加水80 g.
分析 根据溶液中溶质的质量和溶剂质量的计算方法来分析;
根据公式:溶质质量分数=$\frac{溶质质量}{溶液质量}$×100% 一一计算即可.
解答 解:(1)溶质质量=溶液质量×溶质质量分数=80×10%=8g,溶剂质量=溶液质量-溶质质量=80g-8g=72g,故答案为:8;72;
(1)向原溶液中加入40g水,则所得溶液的溶质质量分数为$\frac{8g}{80g+40g}×100%$≈6.7%;故填:6.7%;
(2)向原溶液中加入20g氯化钾固体(固体全部溶解),则所得溶液的溶质质量分数为$\frac{8g+20g}{80g+20g}×100%$=28%;故填:28%;
(3)加水的过程中,溶质的质量不变,所以设加水的质量为x,则
$\frac{8g}{80g+x}×100%=5%$
x=80g
故填:80.
点评 同学们要会根据溶质质量分数=$\frac{溶质质量}{溶液的质量}$×100%灵活计算,要特别注意,溶液质量=溶质质量+溶剂质量.

练习册系列答案
相关题目
13.碳酸钡广泛应用于显像管、光学玻璃等行业.有一种碳酸盐矿石,其主要成分是碳酸钙和碳酸钡.现有该碳酸盐矿石粉末样品(假设杂质不溶于水,也不与盐酸反应),为检验该样品的主要成分,小明同学做了一个实验:取少量样品于烧杯中,加入过量的稀盐酸.
(1)在小明同学的实验中,可观察到的实验现象是固体部分溶解,产生气泡,该实验的目的是检验样品中含有碳酸盐.
(2)在小明同学实验的基础上,请你设计一个实验方案,以进一步证明该碳酸盐矿石的主要成分是碳酸钙和碳酸钡.(本实验条件下,微溶物不形成沉淀)
(1)在小明同学的实验中,可观察到的实验现象是固体部分溶解,产生气泡,该实验的目的是检验样品中含有碳酸盐.
(2)在小明同学实验的基础上,请你设计一个实验方案,以进一步证明该碳酸盐矿石的主要成分是碳酸钙和碳酸钡.(本实验条件下,微溶物不形成沉淀)
| 实验操作 | 预期现象与结论 |
| 取小明同学实验中的少量滤液于烧杯中,向烧杯中 加入过量的稀硫酸,并用玻璃棒搅拌. | 有白色沉淀生成,说明含有硫酸根离子,证明矿石中含有碳酸钡 |
| 向上述实验中的上层清液加入足量的碳酸钠溶液 | 有白色沉淀生成,说明含有钙离子,证明矿石中含有碳酸钙 |
14.为了对氯化钾样品(含KNO3)进行分析,甲、乙、丙三位同学分别进行实验.他们的实验数据如下表,请仔细观察和分析数据,回答下列问题:
(1)该样品中KCl的质量分数是多少?
(2)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的滤液中只含有一种溶质?此溶液的溶质质量分数是多少?
| 项目 | 甲 | 乙 | 丙 |
| 所取固体样品质量(克) | 20 | 10 | 10 |
| 加入AgNO3溶液的质量(克) | 100 | 100 | 200 |
| 反应后所得的沉淀质量(克) | 14.35 | 14.35 | 14.35 |
(2)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的滤液中只含有一种溶质?此溶液的溶质质量分数是多少?
18. 实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
(l)根据步骤①现象,小明得出了该试剂可能为氯化钠溶液或硫酸钠溶液.小明作出该判断的依据是步骤①的实验现象是“无色酚酞试液不变色”.
(2)由步骤②可确定该试剂为硫酸钠溶液.
 实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:
实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如表实验:| 步骤 | 实验操作 | 实验现象 |
| ① | 取5毫升试剂于A试管中,滴入几滴无色酚酞试液 | 无色酚酞试液… |
| ② | 另取5 毫升试剂于B 试管中,滴入几滴氯化钡溶液 | 溶液中出现白色沉淀 |
(2)由步骤②可确定该试剂为硫酸钠溶液.
8.化肥对提高农作物的产量具有重要的作用,碳铵(碳酸氢铵)就是农民朋友经常使用的一种氮肥,碳铵易溶于水、受潮时常温分解,温度越高分解越快,遇碱时放出氨气.某校化学兴趣小组为测定某碳铵肥料样品的纯度,将8.5g样品加入足量的浓氢氧化钠溶液中共热,(碳铵中的杂质不与氢氧化钠反应,反应的方程式为NH4HCO3+2NaOH=Na2CO3+2H2O+NH3↑),把产生的所有NH3用足量的硫酸溶液吸收,同时测量两分钟内硫酸溶液增加的质量,结果如下表所示.
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是不能和碱性肥料混用
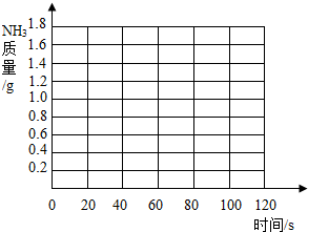
(2)请在如图所示的坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为1.0.
(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)
| 时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是不能和碱性肥料混用
(2)请在如图所示的坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为1.0.

(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)
15.某物质在氧气中完全燃烧只生成二氧化碳和水.据此判断该物质组成说法正确的是( )
| A. | 只含有碳、氢元素基础 | B. | 含有碳、氢、氧三种元素 | ||
| C. | 含有碳、氢元素,可能含有氧元素 | D. | 无法确定 |
 硫酸镁溶液可以和氢氧化钠溶液反应
硫酸镁溶液可以和氢氧化钠溶液反应 SO42-
SO42-  Mg2+
Mg2+  Na+
Na+ 我们在探究物质燃烧的条件时,向在盛有80℃热水的烧杯底部的白磷通入氧气时,奇迹发生了:白磷在水下燃烧起来,写出该化学反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.待温度恢复至室温时,向水中滴加紫色石蕊试液,你预测会显红色,写出发生该现象的化学反应方程式P2O5+3H2O=2H3PO4.
我们在探究物质燃烧的条件时,向在盛有80℃热水的烧杯底部的白磷通入氧气时,奇迹发生了:白磷在水下燃烧起来,写出该化学反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.待温度恢复至室温时,向水中滴加紫色石蕊试液,你预测会显红色,写出发生该现象的化学反应方程式P2O5+3H2O=2H3PO4.