题目内容
7.生产电脑芯片的材料主要是高纯硅,工业生产硅的原理为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,在反应中发生了还原反应的是( )| A. | C | B. | SiO2 | C. | Si | D. | CO |
分析 在氧化还原反应中,氧化剂失去了氧被还原,发生了还原反应;还原剂得氧被氧化,发生了氧化反应,据此进行分析解答即可.
解答 解:根据工业生产硅的原理为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,可知:在此反应中碳得氧发生了氧化反应,是还原剂;SiO2失氧发生了还原反应,是氧化剂.
故选:B.
点评 在化学反应中氧化剂与还原剂往往同时存在,初中阶段一般利用得氧失氧的方法判断,得氧的是还原剂,发生了氧化反应;失氧的是氧化剂,发生了还原反应.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
15.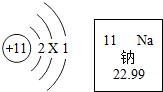 根据如图的有关信息判断,下列说法错误的是( )
根据如图的有关信息判断,下列说法错误的是( )
 根据如图的有关信息判断,下列说法错误的是( )
根据如图的有关信息判断,下列说法错误的是( )| A. | 钠原子的核电荷数为11 | |
| B. | 钠的原子结构示意图中X=8 | |
| C. | 钠原子的相对原子质量为22.99 | |
| D. | 在化学反应中,钠原子容易得到1个电子 |
2.工业生产的纯碱中常常含有一定量的氯化钠.为了测定某批次纯碱中碳酸钠的质量分数,小明同学称取12g纯碱样品放入烧杯中,用相同溶质质量分数的稀盐酸50g,分5次加入,每次充分反应后,称重、计算生成二氧化碳的质量,记录如下:
请回答:
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
| 实验次数 | 稀盐酸用量(g) | 生成二氧化碳的质量(g) |
| 1 | 10 | 1.1 |
| 2 | 10 | 2.2 |
| 3 | 10 | 3.3 |
| 4 | 10 | 4.4 |
| 5 | 10 | 4.4 |
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
12.资源是宝贵的财富,下列有关资源的说法错误的是( )
| A. | 化石燃料是不可再生能源,其中天然气是比较清洁的燃料 | |
| B. | 地壳中含量最高的金属元素是铝,以化合物的形式存在 | |
| C. | 空气是一种宝贵的资源,其中氮气和氧气的体积比约为4:1 | |
| D. | 地球上可利用的淡水资源有限,海水资源丰富,海水中含有80多种金属元素 |
19.化学是一门以实验为基础的科学,下面是我们在初中化学课中经历过的实验.
若按实验中发生的主要化学反应的基本反应类型进行分类,应将待分类组实验归为B组(填字母),你的分类依据是反应物与生成物均为一种单质和一种化合物.
| A组 | B组 | C组 | D组 | 待分类组 |
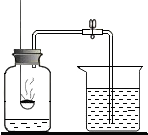 测定空气里氧气的含量 测定空气里氧气的含量 | 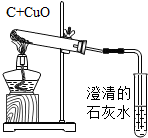 木炭还原氧化铜 木炭还原氧化铜 | 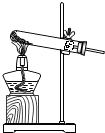 高锰酸钾制氧气 高锰酸钾制氧气 | 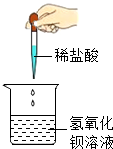 酸碱中和反应 酸碱中和反应 |  铁与硫酸铜溶液反应 铁与硫酸铜溶液反应 |
16.课外实验蕴含着许多有趣的知识,以下课外实验中不涉及化学变化的是( )
| A. |  生成炭黑 | B. |  净水器净化 净水器净化 | C. |  鲜花变色 | D. |  自制汽水 |
 如图是学生经常使用的交通工具.自行车,请完成下列各题:
如图是学生经常使用的交通工具.自行车,请完成下列各题: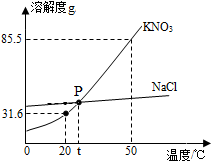 如图为NaCl和KNO3的溶解度曲线,请回答下列问题:
如图为NaCl和KNO3的溶解度曲线,请回答下列问题: