题目内容
3. 研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.实验 | 双氧水的质量(g) | 双氧水浓度(%) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 50 | 6 | 5 | 200 |
| 2 | 50 | 12 | 5 | 100 |
| 3 | 50 | 8 | 5 | 67 |
②实验3中,加入的二氧化锰质量为5g.
③相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
④有同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
⑤加热液体时试管口向上倾斜,加热固体物质时试管口应向下倾斜,原因是防止冷凝水倒流入试管,将试管炸裂.
分析 (1)根据采用的科学研究方法分析解答;
(2)根据题目中提供的数字结合实验是探究双氧水的溶质质量分数对反应速率的影响分析数据;
(3)根据数据分析实验结论;
(4)根据在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯及收集纯净气体的方法分析.
(5)根据加热固体物质时的注意时事项分析.
解答 解:
(1)本实验采用的科学研究方法是控制变量法;
(2)实验探究双氧水的溶质质量分数对反应速率的影响.所以在其他条件相同的情况下进行了三次实验,所以实验3中,加入的二氧化锰质量为5g;其中二氧化锰做催化剂;故填:5;
(3)通过实验中的数据可知,在相同的条件下,双氧水的溶质质量分数越大,反应速率越快,所以相同条件下,实验3产生氧气的速率最快,说明:相同条件下,反应物浓度越大,反应速率越快.故填:双氧水的浓度越大,反应速率越快;
(4)在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯,所以将带火星的木条放在导管口没有复燃;为收集到较纯净的氧气,可以采用排水法收集.
(5)加热液体时试管口向上倾斜,加热固体物质时试管口应向下倾斜,原因是防止冷凝水倒流入试管,将试管炸裂.
答案:
(1)控制变量法;
(2)5;
(3)双氧水的浓度越大,反应速率越快;
(4)排水;
(5)防止冷凝水倒流入试管,将试管炸裂.
点评 催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.

练习册系列答案
相关题目
5.下列图象能正确表示实验过程中相应量的变化关系的是( )
| A | B | C | D |
 |  | 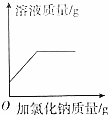 | 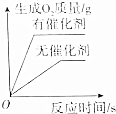 |
| 电解水 | 向pH=2的稀盐酸中加入pH=12的氢氧化钠溶液 | 20℃时,向一定量氯化钠饱和溶液中加入氯化钠固体 | 用等质量氯酸钾分别制取氧气 |
| A. | A | B. | B | C. | C | D. | D |
6.下列家庭小实验不能成功的是( )
| A. | 用食盐水浸泡菜刀除去表面的铁锈 | B. | 用闻气味的方法区别白酒和白醋 | ||
| C. | 用燃烧的方法区别羊毛和涤纶 | D. | 用食醋区别食盐和纯碱 |
10.X、R表示两种金属,在溶液中发生反应:2X+3R(NO3)2═3R+2X(NO3)3,下列说法正确的是( )
| A. | 该反应是复分解反应 | |
| B. | X可能是Fe,R可能是Cu | |
| C. | 若X是Al,R是Cu,则反应后溶液质量减少 | |
| D. | R的金属活动性比X强 |
15.下列生活用品在水中振荡后,不能形成溶液的是( )
| A. | 蔗糖 | B. | 食盐 | C. | 面粉 | D. | 纯碱 |
 某同学设计了如图电解水简易装置,其中A、B电极由金属曲别针制成.通电一段时间后的现象如图所示,则与电源负极相连的是B电极[填A或B],与正极相连的试管内产生的气体是氧气,可用带火星的木条检验.此实验所得的结论有水是由氢元素和氧元素组成的(任写一条即可).
某同学设计了如图电解水简易装置,其中A、B电极由金属曲别针制成.通电一段时间后的现象如图所示,则与电源负极相连的是B电极[填A或B],与正极相连的试管内产生的气体是氧气,可用带火星的木条检验.此实验所得的结论有水是由氢元素和氧元素组成的(任写一条即可). 化学兴趣小组以“酸碱盐的性质”为主题进行探究学习,请你作为小组成员一起来解决下列问题:小红用如图总结了 NaOH的四条化学性质.
化学兴趣小组以“酸碱盐的性质”为主题进行探究学习,请你作为小组成员一起来解决下列问题:小红用如图总结了 NaOH的四条化学性质. 