题目内容
12. (1)配制10%的盐酸的步骤有:
(1)配制10%的盐酸的步骤有:①稀释 ②计算 ③装瓶并贴标签 ④量取浓盐酸和水.其正确的顺序为②④①③(填序号).
(2)配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及玻璃棒.
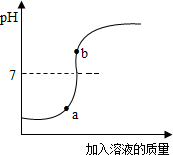
(3)用配得的氢氧化钠溶液与待测的硫酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
a点对应的溶液呈酸性(填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为NaOH和Na2SO4(写化学式).
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(2)实验室配制氢氧化钠溶液操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器进行分析解答.
(3)根据酸性溶液的pH小于7,碱性溶液的pH大于7,酸和碱能发生中和反应生成盐和水解答.
解答 解:
(1)用浓盐酸配制10%的稀盐酸,先计算出所需浓盐酸和水的质量和体积,再量取浓盐酸和水的体积,然后进行溶解,最后进行装瓶并贴标签.
(2)配制氢氧化钠溶液,首先计算配制溶液所需氢氧化钠和水的质量,再称量所需的氢氧化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒.
(3)a点时溶液的pH小于7,溶液呈酸性,b点时溶液的pH大于7,溶液呈碱性,说明溶液含有氢氧化钠,氢氧化钠与硫酸反应生成的是硫酸钠,故溶液中含有硫酸钠,故填:NaOH、Na2SO4.
故答案为:(1)②④①③;(2)玻璃棒.(3)酸性;:NaOH、Na2SO4.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需仪器等是正确解答本题的关键.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
20.化学与人类生活密不可分,下列有关说法错误的是( )
| A. | 室内放一盆水不能防止一氧化碳中毒 | |
| B. | 青少年缺钙会引起佝偻病和发育不良 | |
| C. | 食用甲醛浸泡的食物对人体有害 | |
| D. | 吸烟对人体健康没有影响,因为香烟的烟气中不含对人体有害的物质 |
17.仓库中有一包氮肥的包装标签模糊不清,有同学进行了以下探究:
(1)操作③用玻棒搅拌的目的是使样品充分溶解.
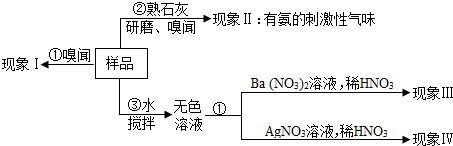
(2)请完成如表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
(3)若现象Ⅲ、Ⅳ都无现象,则该氮肥可能是NH4NO3(写化学式);若操作②现象为无气味、现象Ⅲ、Ⅳ无现象,则该氮肥可能是尿素(只写一种).
(1)操作③用玻棒搅拌的目的是使样品充分溶解.

(2)请完成如表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
| 假设和现象 | 判断和化学方程式 | |
| a | 若现象I为无氨味. | 则样品中不含碳酸氢铵(填名称). |
| b | 由操作②现象判断. | 该样品一定含有铵根离子. |
| c | 若现象Ⅲ为白色沉淀,现象Ⅳ为无沉淀. | 则样品中含有硫酸铵(写名称),该反应的化学方程式为(NH4)2SO4+Ba(NO3)2=BaSO4↓+2NH4NO3. |
| d | 若现象Ⅲ为“无沉淀”,现象Ⅳ为白色沉淀. | 则样品中含有NH4Cl(写化学式),该反应的化学方程式为NH4Cl+AgNO3=AgCl↓+NH4NO3. |
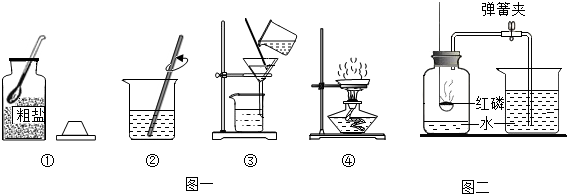
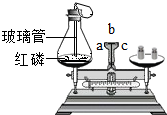 化学课上,同学们用如图所示实验探究质量守恒定律,图中反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,气球的变化情况是先变大后变小,大部分小组同学按老师的要求规范完成实验,发现实验前后,天平的指针都指向b处.但阳光小组同学的天平指针实验前指向b处,实验后指向c处,可能的原因是试验后没有等到冷却锥形瓶冷却就称量(写一种情况即可).小组同学规范了操作后,得到和其它小组同样的结果.实验后,同学们从微观角度分析了化学反应遵守质量守恒定律的原因是化学反应前后原子的种类、数目、质量不变.
化学课上,同学们用如图所示实验探究质量守恒定律,图中反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,气球的变化情况是先变大后变小,大部分小组同学按老师的要求规范完成实验,发现实验前后,天平的指针都指向b处.但阳光小组同学的天平指针实验前指向b处,实验后指向c处,可能的原因是试验后没有等到冷却锥形瓶冷却就称量(写一种情况即可).小组同学规范了操作后,得到和其它小组同样的结果.实验后,同学们从微观角度分析了化学反应遵守质量守恒定律的原因是化学反应前后原子的种类、数目、质量不变.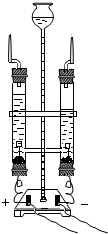 水是生命之源.
水是生命之源.