题目内容
1. 同学们对氢氧化钙的性质进行探究.
同学们对氢氧化钙的性质进行探究.(1)探究氢氧化钙的溶解性.
【实验1】小明向一试管中装入2ml蒸馏水,再加入少许氢氧化钙粉末,充分振荡后得到浑浊的液体,看不出明显的溶解迹象.
【提出问题】氢氧化钙有没有溶解?
【作出猜想】猜想①:氢氧化钙没有溶解;
猜想②:氢氧化钙溶解了,但溶解的量不大.
【实验探究】将“实验1”所得的浑浊液体静置后,取上层清液加入试剂A,根据实验现象证明了“猜想②”成立.你认为试剂A可能是酚酞试液.
(2)探究氢氧化钙能否与盐酸反应.
【实验2】小明向“实验1”中的浑浊液体里加入1mL稀盐酸,观察到不溶物消失,于是得出结论:氢氧化钙能与稀盐酸反应.但同学们讨论后认为小明的结论错误,理由是可能是氢氧化钙溶解于稀盐酸的水里.为此同学们设计了如下实验进行探究.
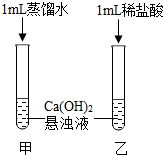
【实验3】按“实验1”重新将氢氧化钙溶于水,并将得到的浊液分成两等份于甲、乙试管内.向甲试管中加入1mL蒸馏水,乙试管中加入1mL稀盐酸(见图).充分振荡后,甲试管内的液体仍然浑浊,而乙中的液体变得清澈.由此得出的结论是:氢氧化钙能(填“能”或“不能”)与稀盐酸反应,化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O(如果认为不反应,则此空不填).
(3)进一步探究:完成“实验3”后,乙试管内的溶质是什么?
【作出猜想】猜想①:是CaCl2; 猜想②:是CaCl2和HCl;猜想③:是CaCl2和Ca(OH)2.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| 向乙试管内的液体中滴加石蕊试液(或碳酸氢钠溶液等); | 溶液显红色(或有气泡产生等). | 猜想②成立 |
分析 (1)氢氧化钙溶于水显碱性来分析解答;
(2)【实验2】根据稀盐酸溶液中有大量水分析;
【实验3】氢氧化钙与稀盐酸反应生成氯化钙和水;
(3)【作出猜想】根据氢氧化钙与稀盐酸反应时可能反应物有剩余,
【实验探究】根据盐酸的性质来分析解答;
解答 解:(1)氢氧化钙溶于水显碱性能使酚酞试液变红色;试剂A可能是酚酞试液;
(2)【实验2】稀盐酸溶液中有大量水,可能是氢氧化钙溶解于稀盐酸的水里;
【实验3】通过对比试验可知,氢氧化钙能与稀盐酸反应,氢氧化钙与稀盐酸反应生成氯化钙和水;
(3)【作出猜想】氢氧化钙与稀盐酸反应生成氯化钙和水,当恰好完全反应时,乙试管内的溶质是氯化钙;
当盐酸有剩余时,乙试管内的溶质是氯化钙和氯化氢;当氢氧化钙有剩余时,乙试管内的溶质是氯化钙和氢氧化钙;
如果猜想②成立,即盐酸有剩余,溶液显酸性,盐酸能使石蕊试液变红色,能与碳酸钠溶液反应产生二氧化碳气体;
答案:(1)【实验探究】酚酞试液;
(2)【实验2】可能是氢氧化钙溶解于稀盐酸的水里;【实验3】能;Ca(OH)2+2HCl═CaCl2+2H2O;
(3)【作出猜想】CaCl2和Ca(OH)2;
【实验探究】石蕊试液(或碳酸氢钠溶液等);溶液显红色(或有气泡产生等).
点评 在做中和反应的实验时,由于酸和碱的溶液一般是无色,二者反应时的现象不明显,所以往往借助于一些试剂或仪器等(如酸碱指示剂、pH试纸、温度计等),来帮助我们判断反应是否进行或恰好完全.

练习册系列答案
相关题目
11.小红对爸爸给患病的奶奶购买的“便携式制氧器”产生了兴趣,她阅读说明书,了解了它的工作原理(如图1)和所用药品.药品中甲剂是一种白色颗粒状固体,作制氧剂;乙剂是黑色固体,作催化剂.甲剂、乙剂和水盛放在图1的反应仓中.

【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢. 可用于制取氧气.
【设计与实验】小红把甲剂和乙剂带到实验室与姜老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小红接着进行如下实验:
【实验一】用甲剂、乙剂和水制取并验证氧气.
(1)根据图1和图2回答问题:
①写出图2中标有a、b的仪器名称:a酒精灯;b试管.
②请指出小红在实验中制取氧气时,应选用的发生装置为B(填字母).
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C(填字母).
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为:2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】检验[实验一]反应后的溶液中是否含有某种离子.
【实验结论】
(1)【实验一】反应后的溶液中一定含有较多钠离子和氯 离子.
(2)甲剂可能是过碳酸钠.

【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢. 可用于制取氧气.
【设计与实验】小红把甲剂和乙剂带到实验室与姜老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小红接着进行如下实验:
【实验一】用甲剂、乙剂和水制取并验证氧气.
(1)根据图1和图2回答问题:
①写出图2中标有a、b的仪器名称:a酒精灯;b试管.
②请指出小红在实验中制取氧气时,应选用的发生装置为B(填字母).
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C(填字母).
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为:2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】检验[实验一]反应后的溶液中是否含有某种离子.
| 实验步骤 | 实验操作 | 实验现象 | 化学反应方程式 |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | |
| 步骤二 | 将步骤一产生的气体通入澄清的石灰水中 | 澄清石灰水变浑浊 | CO2+Ca(OH)2═CaCO3↓+H2O |
(1)【实验一】反应后的溶液中一定含有较多钠离子和氯 离子.
(2)甲剂可能是过碳酸钠.
12.把锌棒插入下列各溶液,过一段时间取出,锌棒质量增加的是( )
| A. | 氯化镁 | B. | 硫酸 | C. | 硫酸铜 | D. | 硝酸银 |
9.下列各组数量关系错误的是( )
| A. | 溶解性:CO2>O2>H2 | B. | 金属活动性:Zn>Fe>Cu | ||
| C. | 氮元素化合价:NO2>N2>NH3 | D. | 溶液的pH:NaOH>HCl>NaCl |
13.除去下列物质中含有的杂质,选用的方法正确的是( )
| 物质 | 所含杂质 | 方法 | |
| A | N2 | O2 | 通过灼热的铜丝 |
| B | CaO | CaCO3 | 加入适量的稀盐酸 |
| C | CO2 | HCl | 通过足量的氢氧化钠溶液 |
| D | NaCl溶液 | Na2CO3 | 加入适量的Ca(NO3)2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
 铁是当前使用最广泛的金属.
铁是当前使用最广泛的金属. 表示氯原子,
表示氯原子, 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)
