题目内容
11.请用元素符号或化学式表示:地壳中含量最多的元素O,氧化铁中铁元素显+3价$\stackrel{+3}{Fe}$2O3,2个氧分子2O2,侯氏制碱法制出的碱Na2CO3.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:地壳中含量最多的元素是氧元素,其符号为:O;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氧化铁中铁元素显+3价,故可表示为:$\stackrel{+3}{Fe}$2O3;
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个氧分子可表示为:2O2;
侯氏制碱法制的“碱”是指纯碱,化学式是 Na2CO3;
故答案为:O;$\stackrel{+3}{Fe}$2O3;2O2;Na2CO3;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
19.保护环境,节约资源,从我做起.下列做法符合这一理念的是( )
| A. | 生活污水直接排放 | B. | 垃圾分类回收处理 | ||
| C. | 废旧电池掩埋在土壤中 | D. | 自来水可以尽情使用 |
16.下列化肥中,从外观即可与其他化肥相区别的是( )
| A. | 氯化钾 | B. | 硝酸铵 | C. | 磷矿粉 | D. | 硫酸钾 |
4.下列属于空气污染物是 ( )
| A. | PM2.5 | B. | CO2 | C. | O2 | D. | N2 |
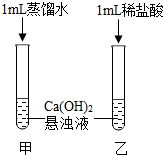 同学们对氢氧化钙的性质进行探究.
同学们对氢氧化钙的性质进行探究.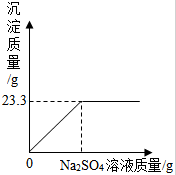 称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
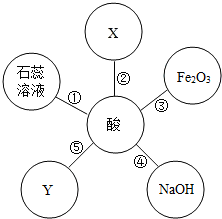 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如下图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.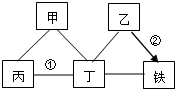 现有铁、碳酸钠、某种红色金属氧化物、稀硫酸和氢氧化钙溶液,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题:
现有铁、碳酸钠、某种红色金属氧化物、稀硫酸和氢氧化钙溶液,它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题: