题目内容
11.小红对爸爸给患病的奶奶购买的“便携式制氧器”产生了兴趣,她阅读说明书,了解了它的工作原理(如图1)和所用药品.药品中甲剂是一种白色颗粒状固体,作制氧剂;乙剂是黑色固体,作催化剂.甲剂、乙剂和水盛放在图1的反应仓中.
【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢. 可用于制取氧气.
【设计与实验】小红把甲剂和乙剂带到实验室与姜老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小红接着进行如下实验:
【实验一】用甲剂、乙剂和水制取并验证氧气.
(1)根据图1和图2回答问题:
①写出图2中标有a、b的仪器名称:a酒精灯;b试管.
②请指出小红在实验中制取氧气时,应选用的发生装置为B(填字母).
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C(填字母).
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为:2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】检验[实验一]反应后的溶液中是否含有某种离子.
| 实验步骤 | 实验操作 | 实验现象 | 化学反应方程式 |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | |
| 步骤二 | 将步骤一产生的气体通入澄清的石灰水中 | 澄清石灰水变浑浊 | CO2+Ca(OH)2═CaCO3↓+H2O |
(1)【实验一】反应后的溶液中一定含有较多钠离子和氯 离子.
(2)甲剂可能是过碳酸钠.
分析 (1)根据反应物的状态和反应条件,可以选择出该反应的装置;
根据收集装置可以确定出气体的性质和收集方法;
(2)只有熟悉氧气的验证方法,才能得出正确的答案.
(3)熟悉反应物、生成物和反应条件,依据化学方程式书写的方法,就能写出正确的化学方程式.
【实验二】考虑二氧化碳与氢氧化钙溶液反应生成碳酸钙和水;
【实验结论】只有熟悉碳酸根离子的检验方法和相关的知识,结合已知条件,就能得出有关问题的正确答案.
解答 解:
【实验一】(1)①图2中标有a、b的仪器名称:a为酒精灯;b为试管.
②根据资料“过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢.可用于制取氧气”,故小红在实验中制取氧气时,应选用的发生装置为B.
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C;
或氧气具有不易溶于水的性质,则可选用的气体收集装置是E;
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】能使澄清石灰水的气体是二氧化碳,二氧化碳与澄清石灰水反应生成碳酸钙沉淀和水,该反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
【实验结论】
(1)【实验一】上述反应说明反应后的溶液跟稀盐酸反应生成了二氧化碳.根据质量守恒定律可知反应后的溶液里含有碳酸根离子.碳酸根含有碳元素和氧元素,说明甲剂中含有钠元素、碳元素和氧元素,或甲剂可能是过碳酸钠.过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢.而碳酸钠和稀盐酸反应生成氯化钠、水、二氧化碳,故反应后的溶液中一定含有较多钠离子和氯离子.
(2)甲剂可能是过碳酸钠.
故答案为:
【实验一】(1)①酒精灯; 试管.②B.③密度大于空气,C.(2)复燃.(3)2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】CO2+Ca(OH)2═CaCO3↓+H2O;【实验结论】氯.
点评 本题起点高,但落点低,审好题结合氧气的性质、制取、验证、制氧气的装置、碳酸根离子的检验和物质的推断,难度较大.

 如表提供了A、B两种物质的溶解度数据,读取信息后回答:
如表提供了A、B两种物质的溶解度数据,读取信息后回答:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 物质A | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| 物质B | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
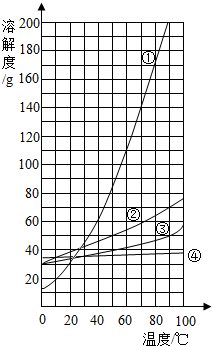
(2)A、B两物质溶解度随温度变化趋势的不同是:A的溶解度变化小,B的溶解度变化大;
(3)如图给出的曲线中,③与A物质溶解度的变化趋势相符(填曲线编号);
(4)从A、B两物质的混合物中分离出B物质,一般采用降温结晶的方法.
| A. | 据质量守恒定律,5g氢气和5g氧气混合点燃充分反应生成水的质量一定是10g | |
| B. | 蒸发20g食盐水后得到2g食盐和18g水,符合质量守恒定律 | |
| C. | 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和 | |
| D. | 镁条在空气中燃烧后,生成物质量比镁条的质量增加了,这违背了质量守恒定律 |
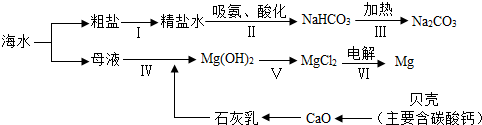
 图为某高钙片标签上的部分文字,请仔细阅读后回答下列问题.
图为某高钙片标签上的部分文字,请仔细阅读后回答下列问题.
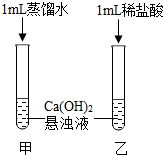 同学们对氢氧化钙的性质进行探究.
同学们对氢氧化钙的性质进行探究.