题目内容
12.把锌棒插入下列各溶液,过一段时间取出,锌棒质量增加的是( )| A. | 氯化镁 | B. | 硫酸 | C. | 硫酸铜 | D. | 硝酸银 |
分析 根据金属活动性顺序及各物质发生化学反应时的质量比来分析作答.在金属活动性顺序表中,氢前面的金属能和常见的酸反生反应置,位于前面的金属能把排在它后面的金属从其盐溶液中转换出来.
解答 解:A、由于锌的活动性要比镁弱,所以把锌棒放入氯化镁溶液中不会发生反应,锌棒的质量不变.
B、把锌棒放入硫酸溶液中,锌棒能和硫酸反应生成可溶于水的硫酸锌和氢气,进入溶液中的发生反应的锌的质量要比逸出的氢气的质量要大得多,因此锌棒的质量会减小.
C、把锌棒放入硫酸铜溶液中,锌能把铜置换出来,由反应时的质量比可知,每65份质量的锌可置换出64份质量的铜,因此锌棒的质量会减轻.
D、把锌棒放入硝酸银溶液中,锌能把银置换出来,由反应时的质量比可,每65份质量的新可置换出216份质量的银,因此锌棒质量增加的.
故选D.
点评 解答本题时要求学生能掌握常见金属的活动性顺序表及其应用,并且根据能发生反应的各物质之间的质量比来进行分析选项.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
3.下列有关叙述正确的是( )
| A. | 据质量守恒定律,5g氢气和5g氧气混合点燃充分反应生成水的质量一定是10g | |
| B. | 蒸发20g食盐水后得到2g食盐和18g水,符合质量守恒定律 | |
| C. | 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和 | |
| D. | 镁条在空气中燃烧后,生成物质量比镁条的质量增加了,这违背了质量守恒定律 |
7.某白色固体甲,可能含有硫酸钠、氢氧化钠、碳酸钠、氯化钠中的一种或几种;某无色溶液乙是初中化学常见的一种可溶性钡盐溶液,为探究它们的成分,进行如下实验,对于固体甲的分析正确的是( )
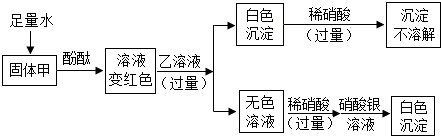

| A. | 一定有硫酸钠、氯化钠 | |
| B. | 一定有氢氧化钠 | |
| C. | 一定有氯化钠 | |
| D. | 至少含有碳酸钠、氢氧化钠中的一种 |
4.下列对一些事实的解释正确的是( )
| 事 实 | 解 释 | |
| A | 铁器比铝器更易生锈 | 铁比铝更活泼 |
| B | 金鱼在冷开水中死亡 | 冷开水中不含氧元素 |
| C | 打开可乐瓶盖冒出大量气泡 | 气体的溶解度随压强的减小而减小 |
| D | 餐具上的油污可用洗洁精洗去 | 洗洁精能够溶解油污 |
| A. | A | B. | B | C. | C | D. | D |
 图为某高钙片标签上的部分文字,请仔细阅读后回答下列问题.
图为某高钙片标签上的部分文字,请仔细阅读后回答下列问题.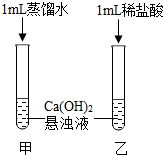 同学们对氢氧化钙的性质进行探究.
同学们对氢氧化钙的性质进行探究.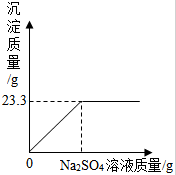 称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入148.8g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题: