题目内容
12.林月和几位同学在实验室用下列装置制取氧气,并进行氧气性质的探究,分液漏斗可以通过调节活塞控制液体滴加速度.试回答下列问题
(1)要收集一瓶较纯净的氧气应选择图中的装置C.(填字母)
(2)某同学在观察到装置B内有大量气泡时,开始用E装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因是集气瓶内根本没收集到氧气或装置漏气
(3)若实验时用过氧化氢代替高锰酸钾加热制氧气,优点是B.(填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
(4)装置B中反应剧烈,据此提出实验安全注意事项是A.
A.控制液体的滴加速度 B.用体积小的溶器 C.加热反应物
(5)林月用高锰酸钾制取氧气,她选择上述装置中的A和C(或E)进行组装.你认为A装置中还缺少一团棉花,该反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(6)做氧气的性质探究时,我用了如下图所示的操作流程.(木炭)

本流程我探究的内容是木炭在氧气中燃烧生成产物是什么.C操作,为了使木炭与氧气完全反应,我的操作方法是将红热的木炭由瓶口向下缓慢插入集气瓶中.
D操作倾倒澄清石灰水的作用是检验生成物,木炭与氧气反应的文字表达式是碳+氧气$\stackrel{点燃}{→}$二氧化碳.
分析 (1)根据排空气法和排水法收集气体的特点进行选择;
(2)根据实验的步骤结合实验的现象分析原因;
(3)根据实验室用高锰酸钾加热制取氧气和过氧化氢溶液制取氧气的不同点逐项分析;
(4)反应很剧烈程度要通过开关调节双氧水的流速;
(5)根据高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气以及反应的注意事项进行解答;
(6)通过对本题图片以及药品的比较来确定本题的解题思路.
解答 解:
(1)因为氧气的密度比空气大,且不易溶于水,因此既可以用向上排空气气法收集氧气,也可用排水法收集氧气,但相对而言,排水法收集到的氧气更纯净;向上排空气法收集的氧气更干燥;故答案为:D;B;
(2)锥形瓶内有大量气泡,但用C装置收集氧气,过一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因是用向下排空气法收集的方法不对,氧气易跑出,使集气瓶内根本没收集到氧气或装置漏气;
故答案为:集气瓶内根本没收集到氧气或装置漏气;
(3)实验过氧化氢溶液制取氧气不需要加热就可发生,且产物只有氧气和水,故答案为:B;
(4)反应很剧烈程度可以通过通过开关调节双氧水的流速,而用体积小的锥形瓶无法控制反应,有可能会由于容积小而导致爆炸;加热反应物则会加剧反应;
故答案为:A;
(5)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,该反应的文字表达方式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;C装置中一处明显的错误是试管口没有放一团棉花;
(6)通过对本题图片以及药品的比较,可以确定本题答案为:木炭在氧气中燃烧生成产物是什么、木炭、将红热的木炭由瓶口向下缓慢插入集气瓶中、检验生成物;木炭与氧气反应的文字表达式是:碳+氧气$\stackrel{点燃}{→}$二氧化碳.
答案:
(1)C
(2)集气瓶内根本没收集到氧气或装置漏气
(3)B
(4)A
(5)一团棉花 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气
(6)木炭在氧气中燃烧生成产物是什么 将红热的木炭由瓶口向下缓慢插入集气瓶中 检验生成物 碳+氧气$\stackrel{点燃}{→}$二氧化碳
点评 化学是一门以实验为基础的学科,因此实验仪器的使用,装置的选择,注意事项,装置的评价,都将是中考热点,解决本题明确实验室制氧气的原理、发生装置和收集方法的选择依据、实验的注意事项等是解答本题关健.

| A. |  向一定量的硫酸铜溶液中加铁粉 | |
| B. |  向一定量pH=2的盐 酸中逐滴加水稀释 | |
| C. |  电解一定质量的水 | |
| D. | 等 质量的锌、铁与足量等浓度稀硫酸反应 |
【提出问题1】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则变质反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解.
【实验探究1】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入足量的氯化钙溶液; | 白色沉淀产生 | 该反应的化学方程式:CaCl2+Na2CO3=CaCO3↓+2NaCl |
| (2)将上述反应后的混合液过滤, 取滤液加入无色酚酞试液. | 酚酞试液变红色 | 证明猜想Ⅱ成立 |
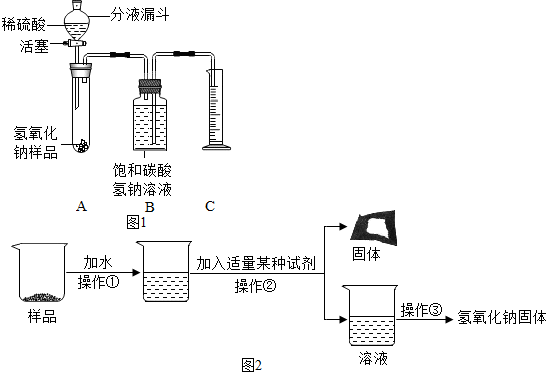
【实验探究2】小红同学设计如图1所示装置(铁架台略去),实验在27℃,101kPa下进行,步骤如下:①按图连接好装置;②用托盘天平准确称取该样品2.0g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢氧化钠溶液220mL.请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是检验装置的气密性;
(2)B中集气瓶盛装的饱和碳酸氢钠溶液不能用水代替,其理由是二氧化碳气体部分溶解在水中影响气体体积的测量;
(3)变质氢氧化钠样品中碳酸钠的质量分数为48%.(在27℃,101kPa时二氧化碳的密度为1.8g/L)(计算结果精确至1%)
【研究与讨论】小明同学认这小红的设计方案过于繁杂,他认为用托盘天平准确称取该样品2.0g后,只需要再称量装置A反应前的总质量(mA前)和完全反应后装置A的总质量(mA后),就能测量出该部分变质样品中碳酸钠的质量分数.
(1)小明认为反应中产生二氧化碳的质量等于mA前-mA后(填数学表达式),从而轻易的计算出该部分变质样品中碳酸钠的质量分数.
(2)小明计算出该部分变质样品中碳酸钠的质量分数的结果数据偏大,请你帮助他分析分析,原因可能是该反应过程中放热反应,导致一部分水以水蒸气的形式逸出.
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】为得到纯净的氢氧化钠固体,小亮设计了如图2所示的实验流程.
请回答下列问题:
(1)操作②中加入的适量某种试剂是氢氧化钙溶液(只写一种);
(2)最终所得氢氧化钠固体质量大于变质后样品中氢氧化钠的质量(填“小于”、“等于”或“大于”).
【实验反思】
实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,请说出其中一个目的:将碳酸钠转化为碳酸钙,以免干扰氢氧化钠的检验.
| A. | CuO | B. | Al2O3 | C. | CaO | D. | ZnO |
| A. | 冰雪融化 | B. | 榨取果汁 | ||
| C. | 点燃酒精加热火锅 | D. | 自行车轮胎爆炸 |
| A. | 浓硫酸暴露在空气中,溶液的质量会变大 | |
| B. | 铝丝表面形成致密的保护膜 | |
| C. | 浓盐酸敞口放置,溶质的质量分数会变小 | |
| D. | 生石灰暴露在空气中会变质 |
| A. | 将气体分别通入澄清的石灰水中 | B. | 观察气体的颜色 | ||
| C. | 将燃烧的木条分别伸入集气瓶中 | D. | 将气体分别通入水中 |

| A. | 在化合物中,①可显-2价,⑤可显+2价 | |
| B. | ①②为非金属元素的原子,④⑤为金属元素的原子 | |
| C. | ③为相对稳定结构,一般不易得失电子 | |
| D. | 上述粒子在发生化学反应时,质子数、电子数均发生改变 |
