题目内容
13.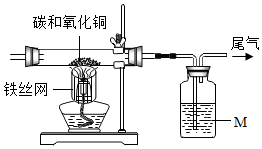 学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按下面的实验装置对木炭与氧化铜的反应进行了实验探究.请你完成下列问题.
学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按下面的实验装置对木炭与氧化铜的反应进行了实验探究.请你完成下列问题.(1)液体M是澄清的石灰水.
(2)酒精灯加上铁丝网罩的作用是提高温度.
(3)现象与解释
| 实验现象 | 用化学方程式解释此现象 |
| ①璃管内黑色粉末逐渐变红 | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ |
| ②澄清的石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H2O |
(5)如果将液体M换成紫色石蕊试液,实验时会看到紫色石蕊试液变红,相关的化学方程式CO2+H2O═H2CO3.
分析 (1)根据二氧化碳的性质分析,
(2)根据反应的条件分析;
(3)根据物质的性质进行分析,木炭具有还原性,能还原氧化铜,生成铜和二氧化碳.
(4)根据木炭的性质分析;
(5)根据二氧化碳与水反应生成碳酸.
解答 解:(1)M验证反应生成了二氧化碳,所以应为澄清的石灰水;
(2)酒精灯加灯罩能提高温度,故填:提高温度;
(3)进行该实验时能看到试管内黑色固体变红,是因为碳与氧化铜反应生成了铜,澄清的石灰水变浑浊是因为该反应生成了二氧化碳,所以:①黑色固体变红,②澄清石灰水变浑浊;化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O.
(4)该实验说明木炭具有还原性,木炭能与氧化铜反应生成铜和二氧化碳.
(5)二氧化碳与水反应生成碳酸,溶液显酸性,如果将液体M换成紫色石蕊试液,实验时会看到紫色石蕊试液变红色,化学方程式为:CO2+H2O═H2CO3.
故答案为:(1)澄清的石灰水[或Ca(OH)2溶液)]
(2)提高温度;
(3)
| 现象 | 用化学方程式解释此现象 |
| ①璃管内黑色粉末逐渐变红 | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ |
| ③澄清的石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H2O |
点评 本题考查了常见物质碳的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列物质长期暴露在空气中,质量会减少的是( )
| A. | 氧化钙 | B. | 氧化铜 | C. | 浓盐酸 | D. | 浓硫酸 |
8.石灰厂为测定一批石灰石样品中碳酸钙的质量分数,取4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中的其它成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥、称量等操作,实验数据如表:
(1)表中X的值为3 g;
(2)该石灰石样品中碳酸钙的质量分数为75%;
(3)计算实验过程中产生二氧化碳气体的总质量.
| 实验 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | X | 2g | 1g | 1g |
(2)该石灰石样品中碳酸钙的质量分数为75%;
(3)计算实验过程中产生二氧化碳气体的总质量.
18.对如表事实的解释中,错误的是( )
| 事 实 | 解 释 | |
| A | 用洗涤剂清洗油污 | 洗涤剂能溶解油污 |
| B | 用水银温度计测量体温 | 温度升高,汞原子间隔变大 |
| C | 用活性炭吸附水中色素 | 活性炭有疏松多孔的结构,具有吸附性 |
| D | 把煤制成“蜂窝煤” | 增大煤与空气的接触面积,使其充分燃烧 |
| A. | A | B. | B | C. | C | D. | D |
5.下列肥料属于复合肥料的是( )
| A. | 硫酸钾(K2SO4) | B. | 磷酸二氢铵(NH4H2PO4) | ||
| C. | 碳酸氢铵(NH4HCO3) | D. | 尿素[CO(NH2)2] |
 人体缺乏维生素C(简称Vc)可能患坏血病,如图为某种“维生素C”说明书的一部分,请回答:
人体缺乏维生素C(简称Vc)可能患坏血病,如图为某种“维生素C”说明书的一部分,请回答:
 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.