题目内容
2.酸、碱、盐是初中化学中的重要物质.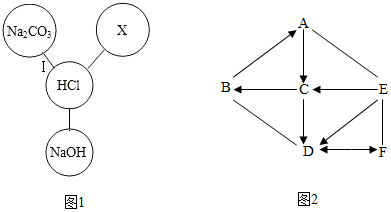
(1)盐酸及时盐化工的重要产品,又是生产硅材料的重要原料,图1归纳出了盐酸与其他物质间相互反应的关系.(图中“-”表示相连的两种物质Ⅰ能发生反应,“→”表示转化)
①若X是与其他三种不同类别的化合物,则X可能是CuO(填化学式);
②根据图1所示物质间关系,写出Ⅰ反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(2)已知A-F六种物质均为初中化学常见物质,其中B、D为氧化物,A、B、E、F为不同类别的化合物,A、B、E放入水中能使酚酞变红,如图是它们之间的关系,请回答:
①写出下列物质的化学式:B是CaO;F可能是H2SO4.
②写出A和E反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;写出B和D反应的化学方程式CaO+H2O═Ca(OH)2.
分析 (1)①根据酸的化学性质,酸能与碱反应,酸能与盐反应,酸能与碱性氧化物反应可解答此题;
②根据复分解反应发生的实质,可以书写化学方程式;
(2)①根据A、B、E放入水中能使酚酞变红,说明三种物质在水中显碱性,B、D为氧化物,A、B、E、F为不同类别的化合物,说明B是氧化钙,A就是氢氧化钙,E是一种显碱性的盐,所以E就是碳酸钠,C就是碳酸钙,D就是水,F是一种强酸,将推出的各种物质验证即可,
②根据推出的反应物、生成物书写化学方程式.
解答 解:(1)①因为我们学过酸的化学性质,酸能与碱反应,酸能与盐反应,酸能与碱性氧化物反应,又因为氢氧化钠属于碱,碳酸钠属于盐,就少了碱性氧化物反应这种类型,所以我们可以选择学过的最常见的碱性氧化物氧化铁、氧化铜等;故答案为:Fe2O3(CuO);
②据复分解反应发生的实质,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)①A、B、E放入水中能使酚酞变红,说明三种物质在水中显碱性,B、D为氧化物,A、B、E、F为不同类别的化合物,说明B是氧化钙,A就是氢氧化钙,E是一种显碱性的盐,所以E就是碳酸钠,C就是碳酸钙,D就是水,F是一种强酸,各种物质都满足转换关系,故答案为:CaO H2SO4
②氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故答案为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
氧化钙和水生成氢氧化钙,故答案为:CaO+H2O═Ca(OH)2.
故答案为:(1)①Fe2O3(CuO);
②Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)①CaO,H2SO4;
②Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
CaO+H2O═Ca(OH)2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

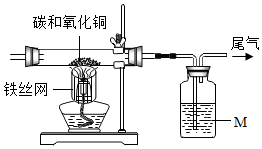 学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按下面的实验装置对木炭与氧化铜的反应进行了实验探究.请你完成下列问题.
学习碳单质的性质时,某校实验小组的同学为探究碳的化学性质,按下面的实验装置对木炭与氧化铜的反应进行了实验探究.请你完成下列问题.(1)液体M是澄清的石灰水.
(2)酒精灯加上铁丝网罩的作用是提高温度.
(3)现象与解释
| 实验现象 | 用化学方程式解释此现象 |
| ①璃管内黑色粉末逐渐变红 | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ |
| ②澄清的石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H2O |
(5)如果将液体M换成紫色石蕊试液,实验时会看到紫色石蕊试液变红,相关的化学方程式CO2+H2O═H2CO3.
| A. | 金刚石、生铁、黄铜都属于金属材料 | |
| B. | 合成材料包括合成纤维、合成橡胶、合金 | |
| C. | 可用抽丝、灼烧、闻气味的方法鉴别羊毛纤维和棉纤维 | |
| D. | 石墨做润滑剂是因为质软 |
| A. | 对水资源要进行保护 | B. | 生活中可通过煮沸降低水的硬度 | ||
| C. | 抑制水中所有动植物的生长 | D. | 河水经沉淀、过滤处理后得到纯水 |
| A. | +1 | B. | +5 | C. | -1 | D. | +7 |
| A. | 某些工业废水处理后可循环使用,以节约水资源 | |
| B. | 为解决“白色污染”问题,应将所有废弃塑料采用焚烧的方法处理 | |
| C. | 禁止秸秆就地焚烧,提倡用秸秆代替煤作燃料进行火力发电 | |
| D. | 积极开发使用风能、太阳能、潮汐能等新能源,减少化石燃料的使用 |
