题目内容
自然界中有一种“雷雨发庄稼”的现象,即在雷雨过后农作物生长得更好.据估计地球上年均发生3l万余次的闪电,每当电闪雷鸣之时,空气中发生的一种反应为:N2+O2
2NO;已知32g氧气和足量氮气化合生成一氧化氮时要吸收180kJ的能量,假设某次闪电放出的能量为1.50×107 kJ,其中有
的能量用于这一反应.求:
(1)此次闪电所产生的一氧化氮的质量是多少千克?
(2)如果此次闪电生成的一氧化氮,在空气中经过一系列变化全部转化为硝酸铵,那么这些一氧化氮相当于多少千克硝酸铵的含氮量?(精确到0.01)
| ||
| 1 |
| 1000 |
(1)此次闪电所产生的一氧化氮的质量是多少千克?
(2)如果此次闪电生成的一氧化氮,在空气中经过一系列变化全部转化为硝酸铵,那么这些一氧化氮相当于多少千克硝酸铵的含氮量?(精确到0.01)
考点:根据化学反应方程式的计算,化合物中某元素的质量计算
专题:有关化学方程式的计算
分析:(1)根据化学方程式计算出32g氧气和足量的氮气反应生成NO的质量,然后根据“1.50×107KJ×
÷180KJ”计算出此次闪电用于这一反应的能量是32g氧气和足量的氮气化合成一氧化氮时要吸收的能量的倍数,再乘以32g氧气和足量的氮气反应生成NO的质量即可;
(2)根据化学式计算可知,此次闪电的生成物NO与硝酸铵的含氮量相等,据此列出比例式,就可计算出硝酸铵的质量.
| 1 |
| 1000 |
(2)根据化学式计算可知,此次闪电的生成物NO与硝酸铵的含氮量相等,据此列出比例式,就可计算出硝酸铵的质量.
解答:解:(1)每次闪电用于生成一氧化氮的能量为:1.50×107 kJ×
=1.50×104 kJ
设32 g氧气和足量氮气化合生成一氧化氮的质量为X.
N2+O2
2NO
32 60
32g X
=
X=60g
设此次闪电所产生的NO的质量是y.
N2+O2
2NO 吸收能量
32g 60g 180 kJ
y 1.50×104 kJ
=
y=5000g=5Kg
(2)此次闪电一氧化氮的相当Z千克硝酸铵的含氮量.
2NO----------NH4NO3;
60 80
5Kg Z
=
z=6.67kg
答:(1)此次闪电所产生的NO的质量是5Kg..
(2)这些一氧化氮相当于6.67千克硝酸铵的含氮量.
| 1 |
| 1000 |
设32 g氧气和足量氮气化合生成一氧化氮的质量为X.
N2+O2
| ||
32 60
32g X
| 32 |
| 60 |
| 32g |
| x |
X=60g
设此次闪电所产生的NO的质量是y.
N2+O2
| ||
32g 60g 180 kJ
y 1.50×104 kJ
| 60g |
| y |
| 180KJ |
| 15000KJ |
y=5000g=5Kg
(2)此次闪电一氧化氮的相当Z千克硝酸铵的含氮量.
2NO----------NH4NO3;
60 80
5Kg Z
| 60 |
| 5kg |
| 80 |
| z |
z=6.67kg
答:(1)此次闪电所产生的NO的质量是5Kg..
(2)这些一氧化氮相当于6.67千克硝酸铵的含氮量.
点评:本题主要考查学生运用化学方程式进行计算的能力.学生需认真分析题意,找出相关联的数据,细心计算,才能正确解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目




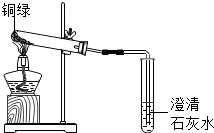 探究首饰中的金属
探究首饰中的金属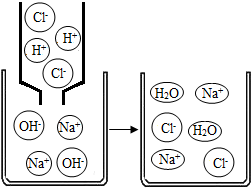 某探究小组的同学用H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液进行“复分解反应发生条件及应用”的实验探究.
某探究小组的同学用H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液进行“复分解反应发生条件及应用”的实验探究. 
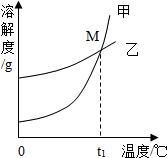 K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.