题目内容
某工厂化验室用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含几滴酚酞试液,质量忽略不计),混合液刚好由无色变成粉红色时,可认为恰好反应.原盐酸中溶质的质量分数为多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:氢氧化钠和盐酸反应生成氯化钠和水,根据氢氧化钠溶液质量、溶质质量分数可以计算氢氧化钠的质量,根据氢氧化钠质量可以计算盐酸中氯化氢的质量,进一步可以计算原盐酸中溶质的质量分数.
解答:解:设原盐酸中溶质氯化氢的质量为x,
NaOH+HCl═NaCl+H2O
40 36.5
16.0g×10.0% x
=
x=1.46g
原盐酸中溶质的质量分数为:
×100%=7.3%
答:原盐酸中溶质的质量分数为7.3%.
NaOH+HCl═NaCl+H2O
40 36.5
16.0g×10.0% x
| 40 |
| 16.0g×10.0% |
| 36.5 |
| x |
x=1.46g
原盐酸中溶质的质量分数为:
| 1.46g |
| 20.0g |
答:原盐酸中溶质的质量分数为7.3%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
端午节是中国的传统节日,吃粽子是端午节的一大特色,小明妈妈准备用以下原料包粽子,其中不能使用的是( )
| A、富硒糯米 |
| B、含锌白糖 |
| C、强化铁酱油 |
| D、甲醛浸泡过的粽叶 |
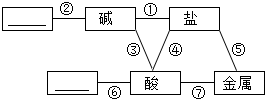 归纳是学习发的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习发的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白: 已知A、B、C、D、E、F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“-”表示两种物质间能发生反应).又知A、B、D都是由两种元素组成,且A、B所含元素各不相同;C、E均含三种元素,其中E常用来改良酸性土壤;F是一种能维持生命活动的单质(通常状态下为气体).请按要求回答下列问题:
已知A、B、C、D、E、F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“-”表示两种物质间能发生反应).又知A、B、D都是由两种元素组成,且A、B所含元素各不相同;C、E均含三种元素,其中E常用来改良酸性土壤;F是一种能维持生命活动的单质(通常状态下为气体).请按要求回答下列问题: