题目内容
2.根据如图五种粒子的结构示意图,回答问题: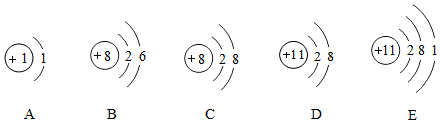
(1)A-E共能表示3种元素.
(2)其中属于稳定结构的有(填序号,下同)CD;属于阴离子的是C.
(3)E 所示的是金属元素(填“金属元素”,“非金属元素”)的原子,其核外有3个电子层,最外层有1个电子.
分析 (1)根据微粒的结构示意图中核内的质子数判断属于几种元素的微粒;
(2)最外层电子数是8的粒子(He是2)是稳定结构.根据核内质子数与核外电子数之间的关系判断属于阴离子;
(3)根据B的微粒的结构示意图,判断质子数、元素的类别;
解答 解:(1)由微粒的结构示意图可知,核内的质子数有3种,所以,图中共表示了3 种元素的微粒.
(2)最外层电子数是8的粒子(He是2)是稳定结构,所以CD属稳定结构.故填:CD.在C的微粒的结构示意图中,核内质子数=8<核外电子数=10,属于阴离子.
(3)由E微粒的结构示意图可知,核内的质子数11,属于钠元素,是金属元素,其核外有3个电子层,最外层有1个电子.
答案:(1)3;(2)CD;C;(3)金属元素;3;1.
点评 主要考查了质子数决定了元素的种类,最外层电子数的多少和原子得失电子的关系,培养学生应用知识解决问题的能力.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
12.生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2会越来越多,因此将CO2转化为O2,不仅有科学意义也有重要的实用价值.据科学文献报道,NiFe2O4在一定条件下既能促进CO2分解又可重复使用.NiFe2O4在此反应中是( )
| A. | 粘合剂 | B. | 制冷剂 | C. | 防腐剂 | D. | 催化剂 |
10.一包白色粉末可能由碳酸钠、硫酸钠和氯化钠中的2种或3种组成.经实验得知其中肯定含有碳酸钠和硫酸钠,为了确定是否含有氯化钠,某同学设计了以下实验.请按该同学的思路填写下表:
| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为H2SO4. | 除去Na2CO3 |
| (2)继续加入足量的B,B为Ba(NO3)2溶液,过滤. | 除去H2SO4 |
| (3)向(2)中的滤液中加入C,C为 AgNO3溶液 | 若有白色沉淀生成,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠. |
17.维生素C是生命活动中不可缺少的营养物质,不同的饮料中维生素C的含量不同.下面是小明同学运用学到的实验方法测定橙汁、果味饮料中维生素C的含量.
【实验目的】测定不同饮料中维生素C的含量.
【实验原理】(1)维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
(2)淀粉遇到碘水变蓝色.
【实验试剂】碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
【实验过程】步骤1:在4支试管中分别盛有3.0mL的下列物质:
①蒸馏水,②标准维生素C溶液,③橙汁,④果味饮料.分别向4支试管中滴加2滴淀粉溶液.
步骤2:用4支相同的胶头滴管分别向①~④支试管中逐滴滴加碘水至刚好变色,并记录滴数.
【实验记录】
试回答下列问题:
(1)你认为小明测定的两种饮料中,③的维生素C的含量较高;
(2)有的同学认为测定物质标准维生素C溶液是多余的,你认为呢?请说明理由:不是多余的,因为测定标准维生素C溶液是确定维生素C含量的标准,以便估算出饮料中维生素C的浓度;
(3)化学实验需要控制变量.下列A B D(填序号)情况会影响到测定结果.
A.每次实验所用饮料的颜色不同
B.量取的被测试物质的体积不同
C.试管的大小不同
D.没有用同一规格的胶头滴管滴加碘水.
【实验目的】测定不同饮料中维生素C的含量.
【实验原理】(1)维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
(2)淀粉遇到碘水变蓝色.
【实验试剂】碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
【实验过程】步骤1:在4支试管中分别盛有3.0mL的下列物质:
①蒸馏水,②标准维生素C溶液,③橙汁,④果味饮料.分别向4支试管中滴加2滴淀粉溶液.
步骤2:用4支相同的胶头滴管分别向①~④支试管中逐滴滴加碘水至刚好变色,并记录滴数.
【实验记录】
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
(1)你认为小明测定的两种饮料中,③的维生素C的含量较高;
(2)有的同学认为测定物质标准维生素C溶液是多余的,你认为呢?请说明理由:不是多余的,因为测定标准维生素C溶液是确定维生素C含量的标准,以便估算出饮料中维生素C的浓度;
(3)化学实验需要控制变量.下列A B D(填序号)情况会影响到测定结果.
A.每次实验所用饮料的颜色不同
B.量取的被测试物质的体积不同
C.试管的大小不同
D.没有用同一规格的胶头滴管滴加碘水.
12.小青看见爸爸种花时把草木灰洒在花盆中作肥料,她查阅资料得知草木灰的主要成分是一种含钾的化合物.于是她取一些草木灰做了以下实验,请你帮助她将下列实验报告填写完整:
[反思]实验过程中产生的废液必须处理后再排放.请你对实验2反应后产生的废液处理提出可行的方法酸化处理至中性再排放.
| 实验 序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
| 实验1 | 探究草木灰的成分 | 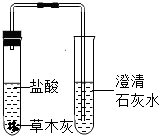 | ①有气泡产生 ②石灰水变浑浊 | 草木灰的主要成分是碳酸钾 |
| 实验2 | 探究碳酸钾的性质 | 向碳酸钾溶液中滴入澄清石灰水 | 有白色沉淀生成 | 化学方程式为K2CO3+Ca(OH)2=CaCO3↓+2KOH |
| 实验3 | 探究实验2反应后上层清液中溶质的成份 | 滴入澄清石灰水 | 有沉淀生成 | 上层清液中有两种溶质 KOH和K2CO3 |
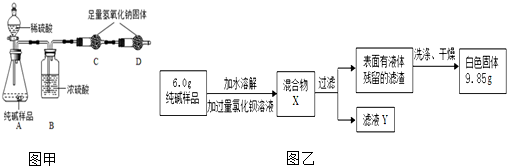
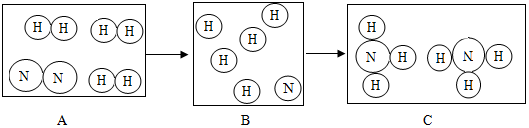
 如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题:
如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题: