题目内容
12.小青看见爸爸种花时把草木灰洒在花盆中作肥料,她查阅资料得知草木灰的主要成分是一种含钾的化合物.于是她取一些草木灰做了以下实验,请你帮助她将下列实验报告填写完整:| 实验 序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
| 实验1 | 探究草木灰的成分 | 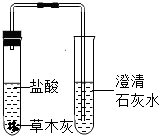 | ①有气泡产生 ②石灰水变浑浊 | 草木灰的主要成分是碳酸钾 |
| 实验2 | 探究碳酸钾的性质 | 向碳酸钾溶液中滴入澄清石灰水 | 有白色沉淀生成 | 化学方程式为K2CO3+Ca(OH)2=CaCO3↓+2KOH |
| 实验3 | 探究实验2反应后上层清液中溶质的成份 | 滴入澄清石灰水 | 有沉淀生成 | 上层清液中有两种溶质 KOH和K2CO3 |
分析 实验一,由结论草木灰的主要成分是碳酸钾及实验方案中的装置和所使用的药品可推测,该实验在检验草木炭中是否含有碳酸根,即该实验的目的;
实验二,碳酸钾与澄清的石灰水即氢氧化钙溶液,可以能过交换成分而发生复分解反应;
实验三,上层清液可能为滴加澄清石灰水量不足时生成的氢氧化钾和未完全反应的碳酸钾的混合溶液,可采取继续滴加澄清石灰水的方法检验;上层清液也可能是滴加过量的氢氧化钙与生成氢氧化钾的混合溶液,可采取滴加碳酸钾的方法检验;
[反思]碱性废液处理时,可加入适量的酸进行中和,酸碱中和能生成盐和水,降低酸性或碱性溶液对环境或生物的影响.
解答 解:实验一:为探究草木灰的成分为碳酸钾,需要向样品中滴加稀盐酸,观察到有气泡产生,试管内的澄清石灰水变浑浊,这些现象说明草木灰为碳酸钾;
实验二:碳酸钾与石灰水的主要成分氢氧化钙交换成分,生成碳酸钙沉淀和氢氧化钾,K2CO3+Ca(OH)2=CaCO3↓+2KOH;
实验三:如果滴加的澄清石灰水不足,上层清液则为碳酸钾和氢氧化钾的混合溶液,采取继续滴入澄清石灰水,若有沉淀生成,即能说明为KOH和K2CO3(或滴入碳酸钾溶液检验澄清石灰水过量;若有沉淀生成;则说明含KOH和Ca(OH)2;其他合理答案均可).
故答案为:
| 实验 序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
| 实验1 | 探究草木灰的成分 | ①有气泡产生; ②石灰水变浑浊 | ||
| 实验2 | K2CO3+Ca(OH)2=CaCO3↓+2KOH | |||
| 实验3 | 滴入澄清石灰水 | 有沉淀生成 | KOH和K2CO3 |
故答案为:酸化处理至中性再排放.
点评 碳酸盐能与酸反应放出气体二氧化碳,实验室通常使用向物质滴加稀盐酸的方法检验物质中含有碳酸根;其中二氧化碳可使用澄清石灰水进行检验.

练习册系列答案
相关题目
20.科学研究时,常常用易观测的量显示不易直接观测的量,下列不是应用这一方法的是( )
| A. |  以不同球说明分子结构 | B. |  以水位表示氧气含量 | ||
| C. |  以水银柱升高判断叶蒸腾快慢 | D. |  以铁屑数目说明磁性强弱 |
7.某有机物在氧气中充分燃烧后,产物只有二氧化碳和水,甲、乙两组学生分别用A、B两种方法测定二氧化碳和水的质量,得到两组数据(如表所示):

请你分析:(1)选用的正确方法应是B(选填“A”或“B”);
(2)由表中数据,推断出这种有机物组成各元素原子的个数比为1:4:1.

| 燃烧有机物质量 | 实验方法 | 实验前后(1)-(4)装置的质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 3.2克 | A | (1)150克 (2)150克 | (1)154.4克 (2)153.8克 |
| 乙组 | 3.2克 | B | (3)150克 (4)150克 | (3)153.6克 (4)154.4克 |
(2)由表中数据,推断出这种有机物组成各元素原子的个数比为1:4:1.
4.某样课外活动小组的同学,在制备有关物质所设计的下列途径中,正确的是( )
| A. | H2$→_{点燃}^{Cl_{2}}$HCl$\stackrel{Na_{2}SO_{4}}{→}$NaCl溶液 | |
| B. | Fe$\stackrel{盐酸}{→}$FeCl3溶液$\stackrel{NaOH溶液}{→}$Fe(OH)3沉淀 | |
| C. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4溶液 | |
| D. | CaO$\stackrel{H_{2}O}{→}$Ca(OH)2溶液$\stackrel{NaCl溶液}{→}$NaOH溶液 |
2.下列有关说法不正确的是( )
| A. | a是胶头滴管,b是试管夹 | |
| B. | 操作中有错误的是步骤一和步骤三 | |
| C. | 步骤二试管中出现的现象是有蓝色沉淀出现 | |
| D. | 滴加硫酸铜溶液时把a伸入试管,以防止液体溅到试管外壁 |

 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.