题目内容
3.分类法是学习化学的重要思想方法,依据同类物质性质的相似性,可以帮助我们做到举一反三.现有下列三组物质:
A.空气、硫酸铜、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | 盐 |
| 不属于上述分类标准的物质 | 空气 | H2SO4 | SO2 |
(3)用上述的物质写一个化学反应方程式(生成物中有二种沉淀)CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
分析 (1)根据物质的组成、分类分析回答;
(2)根据二氧化碳与氢氧化钙的反应,采用类比的方法书写二氧化硫与氢氧化钙反应的化学方程式;
(3)根据物质的性质和题干要求进行书写.
解答 解:(1)碱在水溶液中电离出阴离子全部是氢氧根离子,根据四种物质在水中的电离结果可以判断出,不属于碱的故答案为:B组:H2SO4;
组成中含有金属离子和酸根离子的化合物是盐,将四种物质在水中电离后,只有二氧化硫不满足该条件,故答案为:C组:盐;
(2)二氧化碳和氢氧化钙反应生成碳酸钙和水,二氧化硫和二氧化碳性质比较相似,可以采用类比法书写二氧化硫与氢氧化钙反应的方程式为:SO2+Ca(OH)2═CaSO3↓+H2O;故答为:SO2+Ca(OH)2═CaSO3↓+H2O.
(3)由题干中的物质可知,硫酸铜与氢氧化钡反应生成了硫酸钡沉淀和氢氧化铜沉淀,反应的方程式是:CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓;故答为:CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
点评 能够生成沉淀、气体、水的离子是不能共存的,要学会根据一定的条件对物质进行分类.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
19.下列实验操作正确的是( )
| A. |  过滤 | B. |  点燃酒精灯 | C. |  收集CO2并验满 | D. |  取用液体 |
8. 如图是木炭还原氧化铜的探究实验装置.
如图是木炭还原氧化铜的探究实验装置.
【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:①CO ②CO2 ③CO和CO2.
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
(1)若△m2=0,说明反应产生的气体不被澄清石灰水吸收,则猜想①成立.
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1=△m2(填“>”、“<”或“=”)
【实验并记录】实验得到的数据如下表:
用以上实验数据分析,结果应该是猜想③ 成立.
【反思与评价】经查阅资料知道:木炭还原氧化铜时是产生CO2气体,即反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(1)本次实验结果与资料结果不一致.对其可能原因有同学提出下列分析:
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收
你认为上述分析中合理的是ABCD.
(2)针对分析C,为了提高CO2的吸收效果,可以改进实验,改进的方法是用氢氧化钠溶液代替澄清石灰水.
 如图是木炭还原氧化铜的探究实验装置.
如图是木炭还原氧化铜的探究实验装置.【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:①CO ②CO2 ③CO和CO2.
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | M1 | M2 | △m1即( M1-M2) |
| 烧杯+澄清石灰水 | M3 | M4 | △m2即( M4-M3) |
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1=△m2(填“>”、“<”或“=”)
【实验并记录】实验得到的数据如下表:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 65.4g | △m1 |
| 烧杯+澄清石灰水 | 118.8g | 122.6g | △m2 |
【反思与评价】经查阅资料知道:木炭还原氧化铜时是产生CO2气体,即反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(1)本次实验结果与资料结果不一致.对其可能原因有同学提出下列分析:
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收
你认为上述分析中合理的是ABCD.
(2)针对分析C,为了提高CO2的吸收效果,可以改进实验,改进的方法是用氢氧化钠溶液代替澄清石灰水.
12.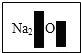 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
[提出问题]这瓶溶液究竟是什么?质量分数是多少?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据残余标签认为一定不可能是氯化钠和硝酸钠.
(2)为了确定该溶液究竟是剩余两种盐的哪一种,及溶液的质量分数他们设计了如下实验.
[设计实验]
[实验结论]该瓶无色溶液是碳酸钠.
(3)该溶液质量分数是多少?
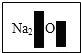 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.[提出问题]这瓶溶液究竟是什么?质量分数是多少?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据残余标签认为一定不可能是氯化钠和硝酸钠.
(2)为了确定该溶液究竟是剩余两种盐的哪一种,及溶液的质量分数他们设计了如下实验.
[设计实验]
| 实验操作 | 实验现象 |
| 取50克少量样品于小烧杯中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 当不再产生沉淀时,将沉淀过滤,称量 | 沉淀的质量为9.85g |
| 向沉淀中滴加稀盐酸 | 产生大量气泡 |
(3)该溶液质量分数是多少?
13.要配制含有K+、Na+、H+、Cl-、SO42-五种离子的溶液,所需要的盐至少有( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
 维生素C主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.计算:人体缺乏维生素C(简称Vc),就会患坏血病.如图是盛放“维生素C”瓶子的标签的一部分,其中维生素C的化学式部分不满,可用C6H8O6表示.根据表中信息回答:
维生素C主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.计算:人体缺乏维生素C(简称Vc),就会患坏血病.如图是盛放“维生素C”瓶子的标签的一部分,其中维生素C的化学式部分不满,可用C6H8O6表示.根据表中信息回答: