题目内容
12.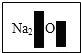 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.[提出问题]这瓶溶液究竟是什么?质量分数是多少?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据残余标签认为一定不可能是氯化钠和硝酸钠.
(2)为了确定该溶液究竟是剩余两种盐的哪一种,及溶液的质量分数他们设计了如下实验.
[设计实验]
| 实验操作 | 实验现象 |
| 取50克少量样品于小烧杯中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 当不再产生沉淀时,将沉淀过滤,称量 | 沉淀的质量为9.85g |
| 向沉淀中滴加稀盐酸 | 产生大量气泡 |
(3)该溶液质量分数是多少?
分析 根据题干提供的信息进行分析,残缺的标签中钠元素的右下角有数字2,且含有氧元素,故不可能是氯化钠和硝酸钠,碳酸钠能与氯化钡反应生成碳酸钡沉淀,碳酸钡沉淀能和盐酸反应产生气体,根据沉淀的质量利用反应的化学方程式求出碳酸钠的质量.
解答 解:(1)氯化钠中不含有氧元素,故不可能是氯化钠;硝酸钠的化学式中钠元素的右下角没有数字2,故不可能是硝酸钠;
(3)根据实验的现象,加入氯化钡产生了沉淀,产生的沉淀能与盐酸反应产生气体,故该物质是碳酸钠,氯化钡能与碳酸钠反应生成碳酸钡沉淀和氯化钠,故填:Na2CO3;
(3)设该溶液中碳酸钠的质量为m
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197
m 9.85g
$\frac{106}{m}=\frac{197}{9.85g}$
m=5.3g
该溶液质量分数是:$\frac{5.3g}{50g}×$100%=10.6%.
答案:
(1)氯化钠和硝酸钠;
(2)碳酸钠;
(3)该溶液质量分数是10.6%.
点评 本题考查了物质的成分的推断,完成此题,可以依据物质的性质结合题干提供的信息进行.

练习册系列答案
相关题目
3.分类法是学习化学的重要思想方法,依据同类物质性质的相似性,可以帮助我们做到举一反三.
现有下列三组物质:
A.空气、硫酸铜、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
(2)请仿照检验CO2的反应,用SO2书写一个类似的化学反应方程式SO2+Ca(OH)2═CaSO3↓+H2O.
(3)用上述的物质写一个化学反应方程式(生成物中有二种沉淀)CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
现有下列三组物质:
A.空气、硫酸铜、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | 盐 |
| 不属于上述分类标准的物质 | 空气 | H2SO4 | SO2 |
(3)用上述的物质写一个化学反应方程式(生成物中有二种沉淀)CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓.
17.明矾的化学式为KAl(SO4)2.12H2O,它的相对分子质量为( )
| A. | 39×27×(32+16×4)×2+12×18 | B. | 39+27+(32+16×4)×2+12×2×1+18 | ||
| C. | 39+27+(32+16×4)×2×12×(1×2+16) | D. | 39+27+(32+16×4)×2+12×(1×2+16) |

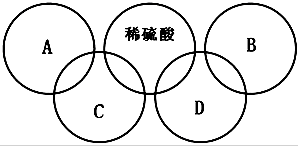 如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.请回答:
如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.请回答: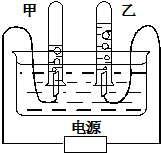 如图表示电解水的简易装置.请回答下列问题:
如图表示电解水的简易装置.请回答下列问题: