题目内容
8.某科学兴趣小组的同学对一份固体样品进行了探究.通过实验已确定该样品由氧化铁和铁粉混合而成,他们称取了13.6g固体样品,用图1所示的装置继续实验,测定的部分数据如图2所示.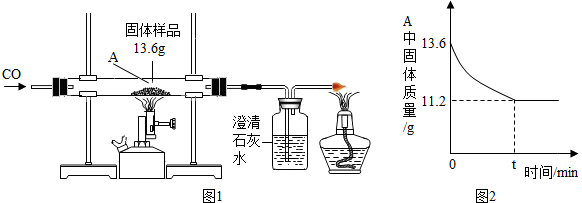
请计算:
(1)固体样品中氧元素的质量是2.4克.
(2)固体样品中氧化铁的质量是8克.
(3)在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
分析 (1)根据题中文字信息和图2提供的数据分析计算;
(2)根据一氧化碳只与氧化铁反应,写出化学反应式,根据提供的数据计算出氧化铁的质量;
(3)根据铁和稀盐酸反应的化学方程式,利用铁的质量计算出生成的溶质氯化亚铁和氢气的质量,根据质量守恒定律计算出溶液的质量,然后根据质量分数公式计算即可.
解答 解:
(1)由于通过实验已确定题中样品由氧化铁和铁粉混合而成,据图1所示的装置实验可知,固体样品中的氧化铁被一氧化碳还原为铁后得到铁粉的总质量为11.2g,所以固体样品中氧元素的质量是13.6g-11.2g=2.4g.
(2)设固体样品中氧化铁的质量为x,则
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 固体减重
160 112 160-112=48
x (13.6g-11.2 g)
$\frac{160}{x}$=$\frac{48}{2.4g}$,解得x=8g
(3)设生成的FeCl2和H2质量分别为x、y,则
Fe+2HCl═FeCl2+H2↑
56 127 2
11.2g x y
$\frac{127}{x}$=$\frac{56}{11.2g}$=$\frac{2}{y}$,解得x=25.4g;y=0.4g
$\frac{25.4g}{(100g+11.2g)-0.4g}$×100%=22.9%.
答:所得溶液中溶质的质量分数为22.9%.
故答案为:
(1)2.4;
(2)8;
(3)22.9%.
点评 本题考查关于化学反应式的计算,需要同学们能够准确的书写化学方程式,理清物质间的关系,才可做出准确的计算.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
18.下列说法中,正确的是( )
| A. | 将100g KCl饱和溶液蒸干得到25g固体,则KCl在该温度下的溶解度为25g | |
| B. | 溶液一定是混合物 | |
| C. | 水能灭火是因为水降低了可燃物的着火点 | |
| D. | 从25%的H2SO4溶液中取出10mL,则取出溶液的质量分数小于25% |
16.对于化学反应X+Na2CO3═2Y+CaCO3↓的分析正确的是( )
| A. | 该反应属于中和反应 | B. | Y中一定含有钠元素 | ||
| C. | X一定是熟石灰 | D. | X中阴离子化合价是-2价 |
3.肼(N2H4)是一种无色油状液体,有刺激性气味,有吸湿性.点燃时,迅速而完全燃烧,生成N2和H2O,并放出大量的热.下列关于N2H4的说法错误的是( )
| A. | 应密封保存 | B. | 完全燃烧的反应不属于置换反应 | ||
| C. | 可用作燃料 | D. | 生成N2和H2O的质量比为7:9 |
20.下列安全措施不正确的是( )
| A. | 燃放烟花爆竹时,远离人群和可燃物 | |
| B. | 天然气泄漏,立即关闭阀门开窗通风 | |
| C. | 正在使用的家用电器着火,立即用水浇灭 | |
| D. | 手持燃着的蜡烛进入山洞发现烛火变弱或熄灭立即退出 |
18.近年来,食品安全成为大家普遍关心的热点问题.从三聚氰胺到地沟油,从毒胶囊到问题奶粉,食品安全问题接连不断,提醒我们要注意食品安全,以确保“舌尖上的安全”,下列加工方法安全的是( )
| A. | 食用小苏打作焙制糕点的发酵成分 | |
| B. | 用红墨水、柠檬黄、果绿等将番薯条染色 | |
| C. | 用工业酒精勾兑水来生产低成本白酒 | |
| D. | 使用超量来硝酸钠作为食品保鲜剂 |
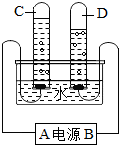 如图为某同学进行电解水实验的装置图,据此回答:
如图为某同学进行电解水实验的装置图,据此回答: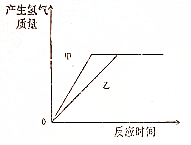 足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.
足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.