题目内容
13.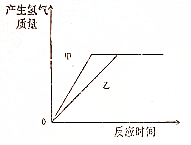 足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.
足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.
分析 根据金属镁和硫酸反应生成硫酸镁和氢气,铁和硫酸反应生成硫酸亚铁和氢气,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,金属的位置越靠前,反应的速率越快进行解答.
解答 解:金属镁和硫酸反应生成硫酸镁和氢气,反应的方程式为Mg+H2SO4═MgSO4+H2↑;铁和硫酸反应生成硫酸亚铁和氢气,反应的方程式为Fe+H2SO4═FeSO4+H2↑;在金属活动性顺序中,氢前的金属能与酸反应生成氢气,金属的位置越靠前,反应的速率越快,在金属活动性顺序中,镁>铁,所以镁的反应速率快,则在图中甲表示镁,乙是铁.故填:Mg+H2SO4═MgSO4+H2↑;Fe+H2SO4═FeSO4+H2↑;镁;镁;铁.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
3.下列物质中,空气中含量最多的是( )
| A. | 氧气 | B. | 氮气 | C. | 稀有气体 | D. | 水蒸气 |
4.2012年3月20日成都市空气质量报告:金牛区空气污染指数为102,空气质量级别为Ⅲ(1)级,空气质量状况为轻微污染,空气首要污染物为可吸入颗粒物,下列有关空气各成分的说法正确的是( )
| A. | 氧气的化学性质比较活泼,氧气属于可燃物 | |
| B. | 氮气的化学性质不活泼,可用于充入灯泡中以延长使用寿命 | |
| C. | 空气质量报告中所列的空气质量级别越高,污染指数越大,表明空气质量越好 | |
| D. | 二氧化碳在空气属于污染物,它在空气中含量增多会引起温室效应 |
18.下列符号能表示两个氮原子的是( )
| A. | N2 | B. | 2N | C. | 2N2 | D. | N2O4 |
5.下列做法不会使人中毒的是( )
| A. | 用工业酒精配制白酒饮用 | B. | 将燃气热水器安装在浴室内 | ||
| C. | 向蔬菜大棚内通入适量的CO2 | D. | 用胆矾对饮用水进行消毒 |
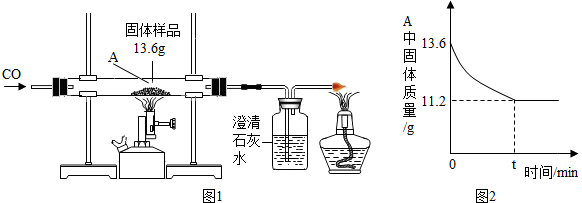
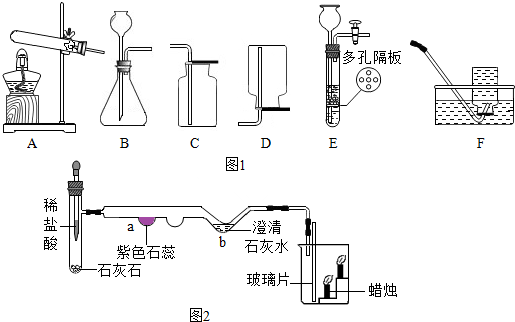
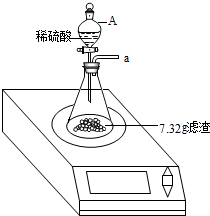 某兴趣小组对月饼包装盒中的“脱氧剂”很好奇,他们观察“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.
某兴趣小组对月饼包装盒中的“脱氧剂”很好奇,他们观察“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.