题目内容
5.A、B两元素的相对原子质量之比为2:1,组成化合物中两元素的质量之比为2:3,则该化合物的化学式为( )| A. | AB | B. | AB2 | C. | AB3 | D. | A2B3 |
分析 根据AB两元素的质量比及相对原子质量之比,可设出化学式来计算原子个数之比来确定化合物的化学式.
解答 解:设化合物的化学式为AmBn,由相对原子质量之比为2:1,
则设相对原子质量分别为2a、a,
根据AB两元素的质量比为2:3,
2a×m:a×n=2:3,
解得m:n=1:3,
即化合物的化学式为AB3,
故选:C.
点评 本题考查化合物忽的化学式的推断,学生应大胆假设,利用正向思维方法来进行元素质量比的计算即可.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
15.某粒子的结构示意图是 ,下列有关说法中,不正确的是( )
,下列有关说法中,不正确的是( )
 ,下列有关说法中,不正确的是( )
,下列有关说法中,不正确的是( )| A. | 该元素原子的核外共有2个电子层 | B. | 该元素是一种金属元素 | ||
| C. | 该粒子是阳离子 | D. | 该粒子的最外电子层具有稳定结构 |
20.给高锰酸钾加热至完全反应,剩余的固体有( )
| A. | 高锰酸钾 | B. | 氧气 | C. | 锰酸钾 | D. | 二氧化锰 |
14. 如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )
 如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )| A. | tl℃时,甲、乙两物质的溶液升到t2℃时,所得溶液的溶质质量分数相等 | |
| B. | t2℃时,甲、乙两物质的饱和溶液降到tl℃时,甲析出的质量比乙大 | |
| C. | 乙中含有少量的甲,可用冷却热饱和溶液的方法提纯乙 | |
| D. | t2℃时,用210g甲的饱和溶液加水可以配制成550g20%的甲溶液 |
15.某化学活动小组用如图所示实验装置探究氨气(NH3)的性质、测定氧化铜试样中氧化铜的质量分数(其中杂质不发生变化,装置中的每一步处理都是完全的),充分反应后观察到C装置中的固体由黑色转变为亮红色.
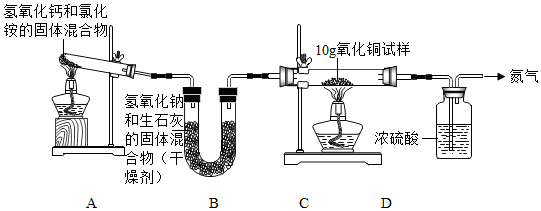
试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
10g氧化铜样品中氧化铜的质量是8g;
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.

试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
| C装置总质量 | D装置总质量 | |
| 实验前 | 160g | 200g |
| 实验后 | 158.4g | 201.8g |
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
 如图是常用气体制备的装置图.
如图是常用气体制备的装置图. 将10%的NaOH溶液逐滴加入20g稀硫酸样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试计算:
将10%的NaOH溶液逐滴加入20g稀硫酸样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试计算: 海水淡化可缓解淡水资源匮乏的问题,如图为太阳能海水淡化装置示意图.
海水淡化可缓解淡水资源匮乏的问题,如图为太阳能海水淡化装置示意图.