题目内容
15.某化学活动小组用如图所示实验装置探究氨气(NH3)的性质、测定氧化铜试样中氧化铜的质量分数(其中杂质不发生变化,装置中的每一步处理都是完全的),充分反应后观察到C装置中的固体由黑色转变为亮红色.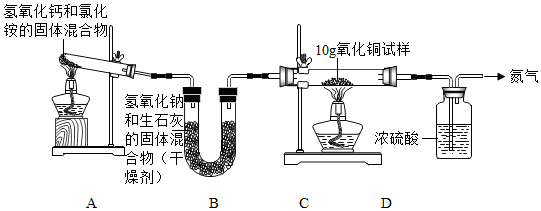
试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
| C装置总质量 | D装置总质量 | |
| 实验前 | 160g | 200g |
| 实验后 | 158.4g | 201.8g |
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
分析 (1)根据气体的性质可以选择收集气体的方法;
(2)为了防止水蒸气冷凝回流炸裂试管,试管口应该略向下倾斜;
(3)C装置中减小的质量是氧化铜中氧元素的质量,D装置中增加的质量是反应生成水的质量;
(4)加热条件下,氧化铜和氨气反应生成铜、水和氮气.
解答 解:(1)氮气的密度和空气相似,不能用排空气法收集,难溶解于水,可以用排水法收集,因此实验室收集氮气的方法是排水集气法.
故填:A.
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管.
故填:防止冷凝水倒流炸裂试管.
(3)设氧化铜的质量为x,
氧化铜中氧元素质量为:160g-158.4g=1.6g,
根据题意有:80:16=x:1.6g,
x=8g,
因此10g氧化铜样品中氧化铜的质量是8g.
故填:8g.
(4)C装置的玻璃管内,氧化铜和氨气反应生成铜、水和氮气,反应的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
故填:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
5.A、B两元素的相对原子质量之比为2:1,组成化合物中两元素的质量之比为2:3,则该化合物的化学式为( )
| A. | AB | B. | AB2 | C. | AB3 | D. | A2B3 |
3.如图为某反应的微观示意图,下列说法不正确的是( )


| A. | 反应后的物质是混合物 | |
| B. | 反应的AB与B2的分子个数比为2:3 | |
| C. | 该反应说明化学为化中分子可分 | |
| D. | 两种元素化合时,原子个数比不唯一 |
4.若用碳酸钠粉末与盐酸反应验证质量守恒定律,从下列装置中,可选择的有( )
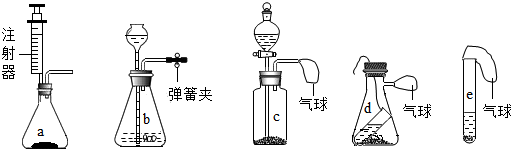

| A. | a、b、e | B. | c、d、e | C. | b、d、e | D. | a、b、c、d、e |
5.下列叙述不正确的是( )
| A. | 铜、铁、银相比导电性最好的是银 | |
| B. | 铁和铝都能跟稀硫酸发生置换反应,铜不可以 | |
| C. | 铁制品非常坚固,不易损坏,不能变质 | |
| D. | 铁器能被磁铁吸引 |
 如图为小明制作的泥水过滤的实验装置图,请指出该装置的错误之处;若改正之后发现滤液仍然浑浊,请分析原因(原因至少两条)
如图为小明制作的泥水过滤的实验装置图,请指出该装置的错误之处;若改正之后发现滤液仍然浑浊,请分析原因(原因至少两条)
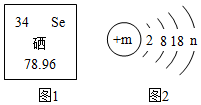 如图1是元素周期表中的一部分,图2是硒原子的结构示意图.据图回答问题:
如图1是元素周期表中的一部分,图2是硒原子的结构示意图.据图回答问题: