题目内容
14. 如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种固体物质(含结晶水)的溶解度曲线,下列叙述正确的是( )| A. | tl℃时,甲、乙两物质的溶液升到t2℃时,所得溶液的溶质质量分数相等 | |
| B. | t2℃时,甲、乙两物质的饱和溶液降到tl℃时,甲析出的质量比乙大 | |
| C. | 乙中含有少量的甲,可用冷却热饱和溶液的方法提纯乙 | |
| D. | t2℃时,用210g甲的饱和溶液加水可以配制成550g20%的甲溶液 |
分析 A、不知升温前溶液中溶质、溶剂的质量,无法判断溶质质量分数大小;
B、不知降温前饱和溶液的质量,无法判断析出晶体质量多少;
C、据甲乙的溶解度受温度影响情况,可分析提纯物质的方法;
D、根据溶解度曲线可知,t2℃时,甲的溶解度是110g进行解答.
解答 解:A、不知升温前溶液中溶质、溶剂的质量,无法判断溶质质量分数大小,若降温前两溶液是饱和溶液溶液、且质量相等则相等,故错误;
B、不知降温前饱和溶液的质量,无法判断析出晶体质量多少,故错误;
C、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,要提纯乙可用蒸发溶剂的方法,故错误;
D、根据溶解度曲线可知,t2℃时,甲的溶解度是110g,其饱和溶液的溶质质量分数=$\frac{110g}{210g}$×100%=52.4%,所以t2℃时,用210 g甲的饱和溶液加水可以配制成550g 20%的甲溶液,正确.
故选:D.
点评 本题主要考查了固体溶解度曲线的意义及温度对固体溶解度的影响,培养学生应用知识解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列实验操作和数据正确合理的是( )
| A. | 用50mL量筒量取2.3mL酒精 | |
| B. | 用湿润的PH试纸测得酸雨样品的PH为5.8 | |
| C. | 不用砝码,直接用托盘天平游码称取小苏打样品4.3g | |
| D. | 量取10mL98%的浓H2SO4慢慢注入10mL水中混合均匀得20mL49%的稀H2SO4 |
5.A、B两元素的相对原子质量之比为2:1,组成化合物中两元素的质量之比为2:3,则该化合物的化学式为( )
| A. | AB | B. | AB2 | C. | AB3 | D. | A2B3 |
19.某小组对H2O2溶液制氧气进行了如下探究:
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
(2)写出有标号仪器的名称:①分液漏斗;②锥形瓶.
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:

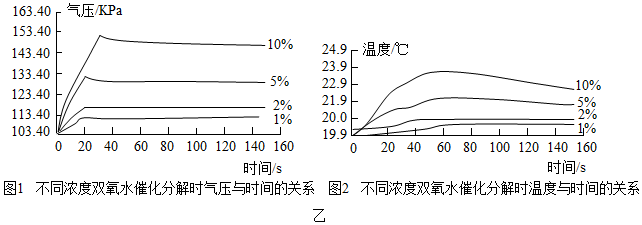
(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
| 催化剂种类 | 气体产生速率(mL/s) |
| MnO2 | 0.03 |
| CuO | 0.07 |
| 活性炭 | 0.12 |
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:


(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
3.如图为某反应的微观示意图,下列说法不正确的是( )


| A. | 反应后的物质是混合物 | |
| B. | 反应的AB与B2的分子个数比为2:3 | |
| C. | 该反应说明化学为化中分子可分 | |
| D. | 两种元素化合时,原子个数比不唯一 |
4.若用碳酸钠粉末与盐酸反应验证质量守恒定律,从下列装置中,可选择的有( )
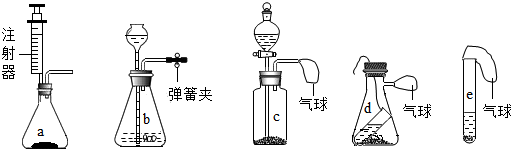

| A. | a、b、e | B. | c、d、e | C. | b、d、e | D. | a、b、c、d、e |

 如图为小明制作的泥水过滤的实验装置图,请指出该装置的错误之处;若改正之后发现滤液仍然浑浊,请分析原因(原因至少两条)
如图为小明制作的泥水过滤的实验装置图,请指出该装置的错误之处;若改正之后发现滤液仍然浑浊,请分析原因(原因至少两条)