题目内容
13.某活动小组的同学将氢氧化钙、纯碱这二种物质混合后加入适量的水搅拌,过滤得到滤渣和滤液,对滤液中溶质的成分进行探究:【猜想与假设】甲同学认为:可能是NaOH、Na2CO3、Ca(OH)2
乙同学认为:可能是NaOH、Na2CO3 丙同学认为:可能是NaOH、Ca(OH)2
丁同学认为:可能是NaOH(填化学式).
【交流与评价】经过讨论,大家一致认为甲同学的猜想不合理.理由是Na2CO3和Ca(OH)2在溶液中不能共存.
【活动与探究】乙同学取原滤液向其中倾倒足量的稀盐酸,观察到有大量气泡产生,于是得出该滤液中溶质是NaOH、Na2CO3的结论,证实了自己的猜想.丙同学取原滤液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原滤液,向其中加入CaCl2溶液观察到有白色沉淀生成,发生反应的化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl,得出了和乙同学相同的结论.丁同学为了验证乙同学结论也取原滤液向其中滴加了少量稀盐酸,却发现无气泡产生.
【解释与结论】大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因.你认为可能的原因是丁同学滴加的盐酸量过少,与氢氧化钠反应.
分析 【猜想与假设】根据实验中的反应物过量进行分析;
【交流与评价】根据物质的共存进行分析;
【活动与探究】根据碳酸钠会与氯化钙反应生成沉淀进行分析;
【解释与结论】根据氢氧化钠会与盐酸反应进行分析.
解答 解:【猜想与假设】反应过程中可能碳酸钠过量,也可能氢氧化钙过量,也可能两者恰好完全反应,故答案为:NaOH;
【交流与评价】碳酸钠会与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故答案为:甲;Na2CO3和Ca(OH)2在溶液中不能共存;
【活动与探究】丙同学取原滤液向其中加入Na2CO3溶液无现象,说明没有氢氧化钙,据此否定了自己的猜想,取滤液加入氯化钙得到了和乙一样的结论,说明存在碳酸钠和氢氧化钠,碳酸钠会与氯化钙生成碳酸钙沉淀,故答案为:有白色沉淀生成;化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl;
【解释与结论】盐酸会与氢氧化钠和碳酸钠反应,如果加入的盐酸量太少,会先于氢氧化钠反应,还没有与碳酸钠反应,故答案为:丁同学滴加的盐酸量过少,与氢氧化钠反应;(或氢氧化钠的量较多与少量的盐酸反应或盐酸与碳酸钠反应生成少量的二氧化碳被氢氧化钠吸收)
故答案为:【猜想与假设】NaOH;
【交流与评价】甲;Na2CO3和Ca(OH)2在溶液中不能共存;
【活动与探究】有白色沉淀生成;Na2CO3+CaCl2═CaCO3↓+2NaCl;
【解释与结论】丁同学滴加的盐酸量过少,与氢氧化钠反应;(或氢氧化钠的量较多与少量的盐酸反应或盐酸与碳酸钠反应生成少量的二氧化碳被氢氧化钠吸收)
点评 在解此类题时,首先分析题中考查的问题,然后结合题中所给的知识和学过的知识进行分析分析解答.

练习册系列答案
相关题目
3.化学反应中常伴随发生一些现象,这些现象可以帮助我们判断化学反应的发生.对下面实验现象的描述中,正确的是( )
| A. | 铜丝在空气中灼烧时,有黑色固体生成 | |
| B. | 氢气在空气中燃烧,发出明亮的蓝色火焰 | |
| C. | 木炭在氧气中燃烧,生成刺激性气味的气体 | |
| D. | 磷在空气中燃烧发出白雾 |
4.下列过程中发生了化学变化的是( )
| A. | 电灯发光 | B. | 水蒸发 | C. | 水果榨汁 | D. | 铁器生锈 |
1.下列科学归类知识有错误的是( )
| A. | 灭火方法 1.森林着火,向火源喷水 2.油锅着火,用锅盖盖灭 | |
| B. | 食品安全 1.工业酒精中含有甲醇等,不能饮用 2.含亚硝酸钠的工业用盐,不能食用 | |
| C. | 实验安全 1.用嘴吹灭燃着的酒精灯 2.将水加入浓硫酸中稀释 | |
| D. | 化学与健康 1.人体缺钙-会影响人体发育 2.人体缺铁-容易引起贫血症 |
2.原子的结构示意图如图,下列叙述正确的是( )
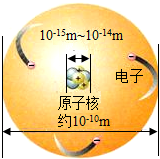

| A. | 原子、中子、电子均匀的分散在原子中 | |
| B. | 质子带正电,电子带负电,但是原子不显电性 | |
| C. | 同一原子中,质子数等于中子数 | |
| D. | 质子与电子质量相等 |
3.水是生命之源,既精通又宝贵.下列对水的“多”与“少”的描述错误的是( )
| A. | 生活中接触的水溶液多,纯净水少 | |
| B. | 我国水资源总量多,人均水量少 | |
| C. | “南水北调”工程说明北方水的储量多,南方水的储量少 | |
| D. | 地球上的水总量多,淡水少 |
 钙是维持人体正常功能所必须的元素,如图所示为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应),烧杯内物质质量变为11.34g.试计算:
钙是维持人体正常功能所必须的元素,如图所示为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应),烧杯内物质质量变为11.34g.试计算: