题目内容
3.有下列装置,请你根据装置图回答下列问题:
(1)实验室加热某固体纯净物制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,应选择的发生装置为B(填字母代号).
(2)小明用锌粒与稀硫酸制取氢气时选用E而没有选用C或D作发生装置,是因为E装置具有的突出优点是便于控制反应的发生和停止;对氢气进行验纯时,发生反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.

(3)实验室用加热氯化铵固体和熟石灰混合物来制取氨气(NH3).氨气是一种有刺激性气味的气体,极易溶于水.若用右图所示装置来收集氨气,氨气应该从b(填“a”或“b”)端进入,为防止氨气污染空气,最好选用F、G其中的G装置来吸收尾气.
分析 (1)根据实验室制取氧气的反应物有过氧化氢溶液和二氧化锰,加热氯酸钾和二氧化锰,加热高锰酸钾,所以加热某固体纯净物制取氧气的高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热进行分析;
(2)根据有孔隔板可以利用气压的作用将固体和液体分离,达到反应停止的目的,氢气和氧气在点燃的条件下生成水进行分析;
(3)根据氨气密度比空气小,极易溶于水进行分析.
解答 解:(1)实验室制取氧气的反应物有过氧化氢溶液和二氧化锰,加热氯酸钾和二氧化锰,加热高锰酸钾,所以加热某固体纯净物制取氧气的高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应的反应物是固体,反应条件是加热,加热高锰酸钾需要在试管口放一团棉花,所以应选择的发生装置为:B;
(2)有孔隔板可以利用气压的作用将固体和液体分离,达到反应停止的目的,所以E装置具有的突出优点是:便于控制反应的发生和停止,氢气和氧气在点燃的条件下生成水,化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)氨气密度比空气小,极易溶于水,所以用右图所示装置来收集氨气,氨气应该从b端进入,为防止氨气污染空气,G装置与水的接触面积大,不会造成倒吸,最好选用F、G其中的G装置来吸收尾气.
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,B;
(2)便于控制反应的发生和停止,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)b,G.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子.下列说法正确的是( )
如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子.下列说法正确的是( )| A. | 有单质生成 | B. | 是化合反应 | ||
| C. | 参加反应的两种分子个数比为4:1 | D. | 反应前后元素的化合价没有变 |
| A. | 稀硝酸 | B. | 稀盐酸 | C. | 氯化钾溶液 | D. | 碳酸钾溶液 |
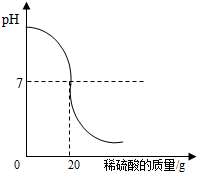 为了测定某氢氧化钠溶液中溶质的质量分数,取氢氧化钠溶液50g,向其中加入溶质的质量分数为4.9%的稀硫酸,加入稀硫酸质量与pH的变化情况如图所示.计算:当加入稀硫酸质量为20g时,所得溶液中溶质的质量分数.
为了测定某氢氧化钠溶液中溶质的质量分数,取氢氧化钠溶液50g,向其中加入溶质的质量分数为4.9%的稀硫酸,加入稀硫酸质量与pH的变化情况如图所示.计算:当加入稀硫酸质量为20g时,所得溶液中溶质的质量分数.



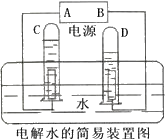 如图是电解水的简易装置.
如图是电解水的简易装置.