题目内容
17.化学是在分子、原子、离子层次上研究物质的性质、组成、结构与变化规律的科学.如图是物质与结构成微粒之间的关系图.回答下列问题:(1)分析上述物质与其构成粒子之间的关系图,空白方框A中应填分子.
(2)铁是由铁原子(填“原子”、“分子”或“离子”)构成的.
(3)氢气的化学性质与氧气的化学性质不同,请从微观的角度分析其原因:氧气和氢气的分子构成不同.
(4)钙原子的结构示意图为
 ,在化学变化中该原子易得到(填“得到”或“失去”)电子,则钙离子的符号是Ca2+.
,在化学变化中该原子易得到(填“得到”或“失去”)电子,则钙离子的符号是Ca2+.
分析 (1)根据已有的知识进行分析,分子、原子、离子是构成物质的基本微粒;
(2)根据物质是由原子、分子、离子构成的解答;
(3)根据氧气和氢气的分子构成不同去分析判断,;
(4)根据最外层电子数小于4个易失去电子.根据离子符号的写法分析解答即可.
解答 解:(1)原子能结合生成分子,故填:分子;
(2)金属铁是由铁原子构成的;
(3)分子可以保持物质的化学性质,氢气的化学性质与氧气的化学性质不同是因为:氧气和氢气的分子构成不同;
(4)由于其最外层电子数是2,小于4所以易失掉电子,使次外层成为最外层,达到8电子稳定结构,从而带两个单位的正电荷,其离子符号为:Ca2+;
答案:
(1)分子;
(2)原子; 离子;
(3)氧气和氢气的分子构成不同;
(4)得到;Ca2+.
点评 本题考查了物质构成的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.元素观是化学的重要观念之一,下列有关元素的说法中错误的是( )
| A. | 元素是具有相同核电荷数的一类原子的总称 | |
| B. | 同种元素的原子核内质子数与中子数一定相等 | |
| C. | 元素周期表,元素的原子序数与该元素原子核电荷数在数值上相同 | |
| D. | 在物质发生化学变化时,原子的种类不变,元素也不会改变 |
12.许多化学物质是一把“双刃剑”,对CO2的利弊评价不同的是,( )
| A. | 利用干冰可进行人工降雨 | |
| B. | 大气层中CO2过多会造成“温室效应” | |
| C. | 大气层中CO2越多,抵御紫外光作用越强 | |
| D. | “碳酸水”浇灌植物对植物光合作用有利 |
2.对下列实验现象的描述不正确的是( )
| A. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 | |
| C. | 红磷在空气中燃烧冒出大量的白烟 | |
| D. | 细铁丝在氧气中燃烧火星四射,生成黑色固体 |
6.现有仪器烧杯、试管、广口瓶、铁架台、集气瓶、止水夹、酒精灯、玻璃片、玻璃棒、燃烧匙、带导气管的橡皮塞,从缺少仪器的角度考虑,下列实验不能进行的是( )
| A. | 空气中氧气体积含量的测定 | B. | 制取氧气 | ||
| C. | 溶解食盐 | D. | 浑浊的水过滤 |
7.海水一是种重要的资源,利用海水可制取镁等物质,有人设计如下实验流程: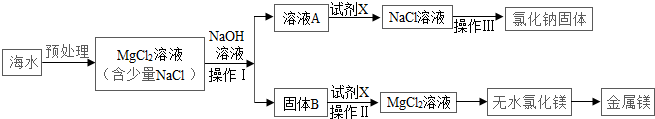
下列说法错误的是( )

下列说法错误的是( )
| A. | 固体B是Mg(OH)2,试剂X为盐酸 | |
| B. | 操作Ⅰ和操作Ⅲ的操作方式完全相同 | |
| C. | 加入NaOH溶液应过量,其目的是使MgCl2完全反应 | |
| D. | 处理等量海水,若将NaOH溶液换成石灰乳,能节约成本 |
 (1)放轻松点,我们来玩一下化学接龙游戏,请注意游戏规则:
(1)放轻松点,我们来玩一下化学接龙游戏,请注意游戏规则: 如图A摘自元素周期表,B是某元素的原子结构示意图,请回答下列问题:
如图A摘自元素周期表,B是某元素的原子结构示意图,请回答下列问题: