题目内容
2.现有10克氢气和氧气的混合气体,点燃后生成了9克水.则原混合气体中氢气和氧气的质量比可能是( )| A. | 1:8 | B. | 1:9 | C. | 1:1 | D. | 1:4 |
分析 根据充分反应后生成9g水,利用化学反应方程式可知,1g氢气和8g氧气恰好完全反应生成9g水,则10g混合气体有剩余的气体存在,则有两种可能:①剩余气体为氢气;②剩余气体为氧气来分析解答.
解答 解:设参加反应反应的氢气和氧气的质量分别为x,y;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,
4 32 36
x y 9g
$\frac{4}{x}=\frac{32}{y}=\frac{36}{9g}$;
解得x=1g,y=8g;
①若剩余气体为氢气,则氢气的质量为1g+(10g-9g)=2g,即混合气体中有2g氢气和8g氧气;则氢气和氧气的质量比1:4;
②若剩余气体为氧气,则氧气的质量为8g+(10g-9g)=9g,即混合气体中有1g氢气和9g氧气,则氢气和氧气的质量比为1:9;
故选BD.
点评 本题考查学生利用化学反应方程式的计算来分析混合物的成分,学生应能利用化学反应判断恰好完全反应的量,要注意过量计算过程的思维训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
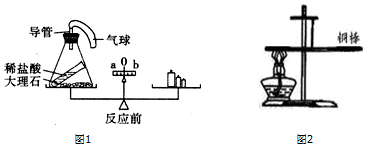
12.某工化肥厂需大量二氧化碳生产化肥,欲购进一批石灰石(其中杂质不参加任何反应),厂家到产地取样分析以确定价格.他们取样2克,并把20克稀盐酸分四次加入,充分反应后,每次剩余固体质量见表
试计算:
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
| 稀盐酸的用量 | 剩余固体的质量/g |
| 第一次加入5g | 1.4g |
| 第二次再加入5g | 0.8g |
| 第三次再加入5g | 0.4g |
| 第四次再加入5g | 0.4g |
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
10.某元素的微粒37X-的核外电子数为18,则该元素原子的中子数是( )
| A. | 17 | B. | 18 | C. | 19 | D. | 20 |
14.下列物质敞口放置在空气中较长时间,无明显变化的是( )
| A. | 浓盐酸 | B. | 生石灰 | C. | 氯化钠溶液 | D. | 浓硫酸 |
9.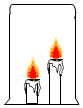 如果遇到火灾,人们可以采用“用湿毛巾(或口罩等)捂住口鼻,蹲下(或匍匐)前行”等逃生方法.根据此求生措施,你推测在两支长短不同的燃烧的蜡烛上方罩一只烧杯(如图所示),能观察到的现象是( )
如果遇到火灾,人们可以采用“用湿毛巾(或口罩等)捂住口鼻,蹲下(或匍匐)前行”等逃生方法.根据此求生措施,你推测在两支长短不同的燃烧的蜡烛上方罩一只烧杯(如图所示),能观察到的现象是( )
 如果遇到火灾,人们可以采用“用湿毛巾(或口罩等)捂住口鼻,蹲下(或匍匐)前行”等逃生方法.根据此求生措施,你推测在两支长短不同的燃烧的蜡烛上方罩一只烧杯(如图所示),能观察到的现象是( )
如果遇到火灾,人们可以采用“用湿毛巾(或口罩等)捂住口鼻,蹲下(或匍匐)前行”等逃生方法.根据此求生措施,你推测在两支长短不同的燃烧的蜡烛上方罩一只烧杯(如图所示),能观察到的现象是( )| A. | 同时熄灭 | B. | 长蜡烛先灭 | C. | 短蜡烛先灭 | D. | 无法确定 |
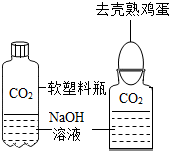 该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?
该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?